
5.5.1* Информоферы
Литература: [223-230]
Каким образом молекулы информатина формируют информофер и ЗОБ-частицу? Этот вопрос детально исследовался Е. М. Луканидиным и В. В. Кульгускиным в экспериментах по диссоциации и реконструкции 30S-частиц. Ранее указывалось, что при переваривании 30S-частиц РНКазой разрушается практически вся входящая в их состав РНК. К сожалению, белки частиц при этом агрегируют и выпадают в осадок (опять же сходным образом ведет себя и ДНП хроматина). Поэтому для изучения организации 30S-частиц этот подход непригоден. Однако, если обработать 30S-частицы растворами NaCl высокой концентрации (~2 М), то белок и РНК диссоциируют, и белок при этом остается в растворе. Чтобы следить за белком, его предварительно метили [1251], проводя его йодирование в составе 30S-частиц. После диссоциации 30S-частиц в 2 М NaCl неожиданно оказалось, что меченый белок седиментирует в сахарозном градиенте примерно с той же скоростью, что и исходные частицы (~30S). Это означало, что, хотя РНК и удалена, частицы по-прежнему сохраняют свою форму и размеры, т. е. информоферы не диссоциируют на цепи информатина (рис. 38). Действительно, при электронной микроскопии свободные информоферы выглядят практически так же, как и 30S-РНП. Однако при ультрацентрифугировании в CsCl (в данном случае несущественно, с формальдегидной фиксацией или без нее), частицы взвешивались при плотности 1,34 г/см3, т. е. действительно РНК из них была удалена. Ни после короткой, ни после длительной метки не удалось выявить какой-либо РНК в составе чистых информоферов.
![Рис. 38. Выделение свободных информоферов и реконструкция рибонуклеосом. а - диссоциация 30S-частиц на РНК и информоферы 30S-частицы, меченные [14С] по РНК, йодировали [1251] (белковая метка), диализовали против 2М NaCl и ультрацентрифугировали через 15-30 %-ный сахарозный градиент в 2 М NaCl. 1 - меченая РНК; 2 - меченый белок; значительная часть последнего образует 30S-частицы, лишенные РНК, или информоферы; Б - ультрацентрифугирование информоферов в градиенте плотности CsCl (с фиксацией или без фиксации формальдегидом) . Плавучая плотность падает до 1,34 г/см3 вместо 1,4 г/см3 у 30s-частиц.](pic/000051.jpg)
Рис. 38. Выделение свободных информоферов и реконструкция рибонуклеосом. а - диссоциация 30S-частиц на РНК и информоферы 30S-частицы, меченные [14С] по РНК, йодировали [1251] (белковая метка), диализовали против 2М NaCl и ультрацентрифугировали через 15-30 %-ный сахарозный градиент в 2 М NaCl. 1 - меченая РНК; 2 - меченый белок; значительная часть последнего образует 30S-частицы, лишенные РНК, или информоферы; Б - ультрацентрифугирование информоферов в градиенте плотности CsCl (с фиксацией или без фиксации формальдегидом) . Плавучая плотность падает до 1,34 г/см3 вместо 1,4 г/см3 у 30s-частиц.
Еще одним важным свойством информоферов явилась их способность к легкой ассоциации со своей или с экзогенной гяРНК при диализе от 2 М NaCl к исходному буферу НМТ. При этом в зависимости от размеров добавленной РНК происходило образование либо ЗОБ-частиц, либо их олигомеров, т. е. удавалось воссоздать не только 30S-частицы, но и структуры, близкие к нативным гяРНП (бусы на нити). Таким образом, концепция информофера и одновременно локализация РНК на поверхности информофера получили полное подтверждение. Здесь, однако, возник ряд осложнений, потребовавших дальнейшей работы.
![Рис. 38. Выделение свободных информоферов и реконструкция рибонуклеосом. в - электронная микроскопия свободных информоферов (негативное контрастирование). По размерам (диаметр ~200 А) и внешнему виду свободные от РНК информоферы очень похожи на рибонуклеосомы; г - реконструкция рибонуклеосом из РНК и свободных информоферов; А - ультраценгрифугирование в сахарозном градиенте свободной меченой гяРНК (1), использованной для реконструкции, и полученных из этой РНК и информоферов 30S-частиц (2). Реконструкцию вели диализом смеси от 2 М NaCl к 0,1 М NaCl, 1 мМ MgCl2, 0,025 М фосфату, рН 7,5. Реконструированные частицы неотличимы от исходных по плавучей плотности (1,4 г/см3 и электронно-микроскопической картине); Б - для реконструкции использовали Леченные [1251] информоферы и немеченую гяРНК размером 6-10S (1) или 12-18S (2). В первом случае образуются мономеры, во втором-димеры рибонуклеосом;](pic/000052.jpg)
Рис. 38. Выделение свободных информоферов и реконструкция рибонуклеосом. в - электронная микроскопия свободных информоферов (негативное контрастирование). По размерам (диаметр ~200 А) и внешнему виду свободные от РНК информоферы очень похожи на рибонуклеосомы; г - реконструкция рибонуклеосом из РНК и свободных информоферов; А - ультраценгрифугирование в сахарозном градиенте свободной меченой гяРНК (1), использованной для реконструкции, и полученных из этой РНК и информоферов 30S-частиц (2). Реконструкцию вели диализом смеси от 2 М NaCl к 0,1 М NaCl, 1 мМ MgCl2, 0,025 М фосфату, рН 7,5. Реконструированные частицы неотличимы от исходных по плавучей плотности (1,4 г/см3 и электронно-микроскопической картине); Б - для реконструкции использовали Леченные [1251] информоферы и немеченую гяРНК размером 6-10S (1) или 12-18S (2). В первом случае образуются мономеры, во втором-димеры рибонуклеосом;
Оказалось, что если использовать не мечение [lZ0l] in vitro, а включение меченых аминокислот in vivo, то после диссоциации в 2 М NaCl информоферы распадаются на молекулы информатинов. Можно было предположить, что химические реакции, идущие при йодировании, каким-то образом стабилизируют информофер, например, за счет образования S-S-связей между разными цепями информатинов. Для дальнейшего исследования вопроса ЗОБ-частицы были получены в высокой концентрации и после диссоциации в 2 М NaCl исследованы с помощью аналитического ультрацентрифугирования. При этом было обнаружено, что в растворе 2 М NaCl существует обратимое равновесие информофер-информатины, причем, естественно, чем выше концентрация белка, тем выше содержание информоферов. Взаимодействие молекул информатинов между собою строго кооперативно, так как никаких других компонентов, кроме информатинов и дискретного пика информоферов, не выявляется. Итак, между информоферами и информатинами в 2 М NaCl существует обратимое равновесие. При этом йодирование информоферов блокирует их диссоциацию.
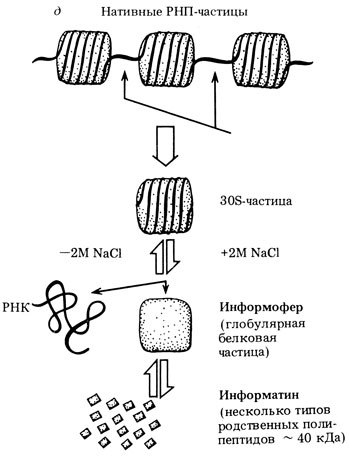
Рис. 38. Выделение свободных информоферов и реконструкция рибонуклеосом. д - схема опыта по реконструкции и повторной диссоциации рибонуклеосом из нейодированных белков и РНК. В 2 М NaCl белки нейодированных рибонуклеосом находятся в зависящем от конценцентрации равновесии между информоферами и одиночными цепями информатина. Только реконструкция с информоферами дает 'правильные' рибонуклеосомы, способные к последующей диссоциации на РНК и белок (по результатам, полученным Е. М. Луканидиным и соавт.)
Если вести реконструкцию 30S-частиц с РНК при высокой концентрации белка, т. е. когда в растворе преобладают информоферы, то образуются 30S-частицы, по свойствам идентичные исходным. Они способны снова диссоциировать в 2 М NaCl и полностью чувствительны к РНКазе. Однако реконструкция, выполненная при низкой концентрации белка (в растворе - свободный информатин), хотя и ведет к формированию 30S-частиц, но эти частицы отличаются от нативных устойчивостью к РНКазе и 2 М NaCl. Иными словами, молекулы информатина обладают сродством к РНК и взаимодействуют с нею, но укладка их в глобулу не носит упорядоченного характера, и РНК более не располагается на поверхности частицы.
Выводы исследований Е. М. Луканидина были далее проверены в группе О. П. Самариной. Молекулы информатина в составе 30S-частиц специально сшивали между собою с помощью обычно используемых для белок-белковых сшивок химических реагентов и тем самым полностью исключали возможность их диссоциации на каком-либо этапе выделения свободных информоферов. Несмотря на это, РНК легко удалялась из 30S-частиц и далее легко проходила реконструкция 30S-частиц или олигочастиц из гяРНК и свободных зашитых информоферов. Эти опыты исключают какой-либо иной тип укладки РНК в 30S-частице, кроме как наматывание на поверхность последней.
В то же самое время О. П. Самариной и сотрудницей физической лаборатории О. Ф. Борисовой велись исследования состояния РНК в 30S-частицах и в растворе с помощью оптических и флюоресцентных методов. Не входя в их детали, укажу на основной вывод из этой работы. Оказалось, что в РНК в составе 30S-частиц исчезает большая часть двухцепочечных участков, которые есть в свободной РНК, происходит плавление вторичной структуры РНК. Это не касается только длинных (100-200 нуклеотидов) двухцепочечных участков в РНК, которые вообще оказываются не связанными с информоферами. В связи с этим следует напомнить, что информатины являются предшественниками белков клетки, вызывающих плавление вторичных структур в нуклеиновых кислотах.
Таким образом, РНК не только наматывается на поверхность информофера, но при этом переходит на большей части своей длины в одноцепочечное состояние. Скорее всего, укладка РНК на поверхности информофера должна носить упорядоченный характер (например, в форме спирали). Можно посчитать, что если длина 600-нуклеотидного отрезка РНК равна 300-400 нм, а диаметр информофера составляет ~20 нм, то на поверхности информофера уложится около шести витков РНК.
Что дает подобная организация РНП-частиц? Во-первых, резкую (15-20-кратную) редукцию линейных размеров, если исходить из длины вытянутой РНК. Во-вторых, доступность всей молекулы РНК действию ферментов процессинга и разным регуляторным факторам. Не исключено, что имеются и другие, более специфические функции, прямо вытекающие из организации 30S-частиц.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'