
Глава 8. Генная инженерия - сельскому хозяйству
Генноинженерные методы наиболее перспективны в сельском хозяйстве, особенно в растениеводстве. Растения очень удобный объект для генных инженеров.
Клетки высших растений, в том числе и культурных, можно размножать на твердой и жидкой среде в культурах. Мы уже писали, что так теперь размножают, кроме микроорганизмов, и клетки высших животных, например человека. Наилучший эффект давали среды с экзотическими добавками, вроде молока кокосового ореха. Теперь разработаны среды дешевые и надежные, позволяющие наращивать большую биомассу растительных клеток с неизмененными свойствами. Все вы слыхали о "корне жизни" - женьшене, из которого получают чудодейственные лекарства. Оказалось, что выгоднее клетки женьшеня наращивать искусственно, в ферментерах, а не создавать плантации (и тем более искать в дальневосточной тайге).
К культивируемым растительным клеткам применимы все методы промышленной микробиологии, включая отбор клеток, интенсивно синтезирующих нужное вещество. Так были получены штаммы клеток растений раувольфии змеиной - продуцента алкалоидов, снижающих кровяное давление, руты душистой, вьюнка, наперстянки, мяты и многих других. В Японии научились растить на искусственной среде клетки шелковицы, а потом их добавлять в синтетические корма для тутового шелкопряда. Это в принципе позволяет разводить шелковичных червей где угодно, даже на Северном полюсе. Оказалось, что шелкопряды могут есть самый разнообразный корм, лишь бы от него пахло шелковицей.
Но главное даже не в этом. Растительные клетки, в отличие от животных разводимые в культуре, сохраняют способность в соответствующих условиях дифференцироваться, превращаться в целое растение, которое можно потом высаживать и размножать семенами. Клетки в культуре можно сохранять в жидком азоте десятки и сотни лет, а затем превращать в целые растения и возвращать на поля. В клеточных культурах гораздо быстрее вести отбор на продуктивность, устойчивость к вредителям и отбирать нужных мутантов. Наконец, в культуры клеток очень удобно встраивать чужие гены, а затем получать растения с нужными свойствами.
Затруднение в том, что растительные клетки, как и клетки дрожжей, одеты в прочные и труднопроницаемые оболочки. Но растительную клетку, как и дрожжевую, можно "раздеть", обработав ферментами, гидролизующими целлюлозу. Так получают протопласты, доступные для внешних воздействий, например трансфекции плазмидами. Потом протопласт сам по себе восстанавливает оболочку и превращается в нормальную клетку.
Протопласты в культуре могут сливаться. Так можно гибридизовать клетки, причем не только одного вида. Гибридизуются и животные клетки: в культуре получены гибридные клетки мыши и крысы, мыши и человека и даже человека и комара. В отличие от животной единичную клетку растения можно превратить в целый организм. Так были получены гибриды разных видов табака, картофеля, томата, петунии, белладонны, моркови, сои и гороха, гороха и бобов. Но межсемейственные гибриды превратить в целые растения не удается: слишком разные геномы объединяются в гибридной клетке, поэтому таким способом нельзя вырастить "на вербе груши". К тому же такой путь не очень перспективен: как вы знаете из первой главы, кроме нужного гена, мы получаем тысячи ненужных. Перспективнее генноинженерный путь: вставка отдельно взятого гена или системы генов, интегрированных в векторе. Культуры клеток и тканей растений открывают путь к решению сверхважной для сельского хозяйства проблемы. Ее можно выразить двумя словами: "безвирусное растениеводство".
Как освободить растения от вирусов. Растения могут поражаться многими сотнями вирусов. Обычно это РНК-содержащие вирусы, хотя, как выше отмечалось, в недавнее время открыты и ДНК-вые. Не все фитовирусы убивают растение, но практически все резко снижают рост, развитие и урожайность. Особенно страдают от фитовирусов те растения, которые размножаются вегетативно - клубнями, как картофель, луковицами, как тюльпаны, черенками и прививками, как смородина и яблоня. Это понятно: перевиваемый черенок из поколения в поколение заражается разными вирусами. Убытки от фитовирусов исчисляются миллиардами.
Сравнительно простой способ получения безвирусных, здоровых растений - выращивать их из отдельно срезанных верхушечных почек, не успевших еще заразиться от старых клеток. Здесь с успехом можно применить культуры клеток и тканей. Однако как узнать, здорова клетка или она содержит вирус?
Диагностика фитовирусов разработана хорошо. В принципе она не отличается от обнаружения вирусов человека и животных. Впрыскивая кролику фитовирус, можно получить антитело на оболочечный антиген вируса. Антисыворотка на вирус - хороший, весьма чувствительный индикатор присутствия вируса в клеточном соке испытуемого растения. Современные методы иммунодиагностики с применением изотопов позволяют обнаружить вирус, если его концентрация даже менее 0,1 мкг/ мл.
Чтобы получить антитела к фитовирусу, надо иметь его оболочечные антигены, т. е. выделять вирус в больших количествах. Тут и приходит на помощь генная инженерия. Ведь целый вирус нам не нужен, требуется лишь его оболочечный белок - антиген. Ген этого белка можно вставить в плазмиду и размножить в бактерии. Этот путь выгоднее, чем наращивать вирус в больных растениях граммами. Первые успехи уже имеются: в МГУ и Институте молекулярной биологии АН СССР клонированы ДНК-копии ряда генов вирусов картофеля. (Напомним, что эти вирусы содержат РНК; чтобы вставить их в геном бактерии, нужно получить кДНК ревертазой.) Так получают антигены. А для получения антител очень перспективны гибридомы, о которых мы уже говорили.
Кроме иммунодиагностики есть и другие методы обнаружения вирусов. PKH или кДНК вируса можно прямо гибридизовать с денатурированной ДНК, выделенной из клетки растения. Такие методы успешно разрабатываются в МГУ, в лаборатории И. Г. Атабекова.
Что нам может дать безвирусное растениеводство? Возьмем для примера картофель. Урожайность безвирусного картофеля в 2 раза выше обычного (200 ц/га вместо средних 100 ц/га), а такая рассада вполне окупает расходы. Следовательно, можно, не снижая объема продукции, вдвое сократить площади под картофель, использовать под него рыхлые почвы, пригодные для картофелеуборочных комбайнов. Если перевести на безвирусность еще и культуры плодовых и ягодных растений, сахарной свеклы, винограда, хмеля, цитрусовых, то можно будет сказать, что получение безвирусных растений - самое важное из того, что дало культивирование клеток.
Безвирусное растениеводство нельзя свести к временной кампании, пока все вирусы не исчезнут с лица Земли. Этого придется ждать бесконечно долго: ведь многие фитовирусы поражают и культурные, и дикие растения-сорняки, а переносят их насекомые и клещи. Поэтому наряду с получением безвирусных растений генетики и генные инженеры работают над выведением новых сортов, вообще устойчивых к вирусам. Есть идея вставить в геномы растений гены интерферонов животных. Первые опыты в этом направлении уже ведутся.
Речь идет не только об интерферонах! Бельгийским ученым удалось вставить в геном табака ген токсина бациллы Бациллюс турингиензис, ядовитого для насекомых. В результате табак приобрел устойчивость к насекомым-вредителям. Значит, в будущем можно будет обойтись без инсектицидов, опасных для человека.
Азотные удобрения и сельское хозяйство. Достижения генной инженерии можно показать еще на одном очень ярком примере. В сельском хозяйстве таким примером может быть проблема фиксации атмосферного азота.
Каждая клетка человеческого организма для того, чтобы синтезировать белки, требует определенного набора готовых аминокислот. Их источником служит растительная и животная пища. Большинство растений синтезируют свои аминокислоты из простейших азотистых соединений - солей аммония и азотной кислоты, содержащихся в почве, на которой они растут. Без подходящего источника азота развитие растений становится невозможным, а без растений была бы невозможной жизнь животных и человека.
Человек издревле использовал азотистые удобрения, стараясь повысить урожайность сельскохозяйственных растений. До середины XIX в. это были природные удобрения, в которых необходимые для растений азотистые вещества образуются главным образом благодаря разложению микроорганизмами остатков растительного и животного материала. В бескислородных условиях бактерии-анаэробы сбраживают органические вещества, и азот освобождается в виде аммиака и аминов; в кислородной атмосфере другие бактерии - аэробные - окисляют амины до аммиака. Часть его улетучивается, другая окисляется дальше с образованием селитр - калиевой и натриевой солей азотной кислоты.
Селитры - прекрасное азотное удобрение, но до XIX в. в Европе для этой цели их не применяли, потому что селитряных месторождений на территории Европы с ее дождливым климатом практически нет. Ведь нитраты легкорастворимы и вымываются из почвы быстрее, чем накапливаются. Но калиевая селитра - главный компонент дымного пороха, без которого немыслима была война. Селитру для пороха добывали, промывая землю из овчарен и хлевов, могильных склепов, погребов и пещер, населенных летучими мышами, - словом, из тех защищенных от дождя мест, где в почве много органических веществ.
Вот почему в Европе широкую известность приобрело открытие в Чили на побережье Тихого океана и прилегающих островах огромных залежей гуаноокаменевшего помета морских птиц, более чем наполовину состоящего из натриевой и калиевой селитр. Дожди в этих краях идут не каждый год и нитраты не вымываются. Древние инки с незапамятных времен задолго до прихода испанцев использовали гуано как удобрение, получая с его помощью богатейшие урожаи кукурузы.
Европейцы стали выделять из гуано калиевую селитру для пороха. В этом была трудность: ведь в этой породе значительно больше натриевой селитры, которая жадно впитывает влагу из воздуха, расплывается и для пороха не годится. Но изобилие гуано окупало трудности по выделению "индийской селитры" (напомним, что из-за ошибки Колумба Америку долго называли Вест-Индией). Индийская, или, как теперь ее называют, чилийская, селитра была важнейшим стратегическим сырьем. Поэтому блокада молодой французской республики в 1793 г. поставила якобинскую революцию перед катастрофой: ведь для республиканской армии требовалось семнадцать миллионов фунтов селитры в год! Республиканскую, а впоследствии и наполеоновскую армии спасли от поражения ученые Г. Монж и К. Бертоле, возродившие старые способы добычи селитры из почв, богатых органикой.
В конце XIX в. интенсивное сельское хозяйство в Европе было немыслимо без чилийской селитры. Но запасы ее были не бесконечны. Пессимисты уже предсказывали истощение запасов, падение урожаев и голод. А ведь немало селитры шло и на нужды развивающейся химической промышленности, в первую очередь на получение азотной кислоты. Сама по себе селитра с появлением бездымного пороха добавлялась лишь в быстро- сгорающие его сорта (пушечный порох). Но азотная кислота оказалась незаменимым сырьем при получении как нитроцеллюлозного пороха, так и практически всех взрывчаток (нитроглицерин и тринитротолуол, мелинит и др.). Однако потребность в азотных удобрениях перекрывала все прочие нужды.
Интересно, что над каждым гектаром посевов, страдающих от недостатка азотистой пищи, находились практически неисчерпаемые запасы азота, потенциально способные снабжать эти посевы в течение многих миллионов лет. Действительно, в атмосфере Земли, на 78% состоящей из азота, содержится около 4х1015 т этого драгоценного элемента. Над каждым гектаром почвы на нашей планете поднимается столб воздуха, содержащий 80 тыс. т азота!
Однако ни одно высшее зеленое растение на Земле неспособно само по себе превратить этот азот в асиммилированную форму. Перед химиками встала задача разработки промышленного способа фиксации азота атмосферы и превращения его в производные аммиака и азотной кислоты. Теория подсказывала, что выгоднее всего связывать азот с водородом, получая аммиак. Соли аммония и раствор аммиака в воде сами по себе хорошее удобрение, а окисляя NH3, можно получать и селитру.
Впервые процесс получения аммиака путем восстановления азота воздуха водородом
разработал в 1904-1907 гг. немецкий химик Ф. Габер. Метод Габера реализовал в производстве в 1913 г. инженер К. Бош.
Метод Габера-Боша лег в основу современной промышленности азотных удобрений. Получающийся на первом этапе из азота воздуха аммиак может быть превращен в селитру, мочевину и другие формы, усвояемые растениями.
Казалось, что проблема азотных удобрений решена. Ведь запасы азота в атмосфере неисчерпаемы. Водород для производства аммиака получают в результате простого и эффективного процесса - конверсии природного газа (метана), запасы которого также еще недавно казались неисчерпаемыми:
Правда, молекула атмосферного азота (N2) - крепкий "орешек". Само восстановление азота водородом приходится вести в довольно жестких условиях - при температуре 450-550°С и давлении 300 атмосфер. И даже эти температура и давление оказались бы недостаточными, если бы не предложенный Ф. Габером катализатор, ускоряющий реакцию, - губчатое железо с добавками окислов калия и алюминия. Катализатор делал энергоемкий процесс связывания азота выгодным до тех пор, пока цены на нефть были низкими.
Однако неумеренное применение азотных удобрений вызвало к жизни новую серьезную проблему. Их эффективность оказалась неожиданно низкой. Вспомним, что нитраты легкорастворимы. Как правило, не меньше половины внесенных в почву селитр вымывается дождями и накапливается в водоемах. Это приводит к "цветению" прудов и озер: в них бурно развиваются микроскопические водоросли, отчего вода становится похожей на зеленые щи. Рыба в таких прудах гибнет. К тому же соли азотной кислоты в высоких концентрациях канцерогенны. С незапамятных времен в колбасы и ветчину добавляли селитру для того, чтобы мясо обрело красивый розовый цвет. Теперь такие добавки категорически запрещены. Кроме того, химические удобрения влияют отрицательно на сообщества почвенных микроорганизмов и в конечном счете вызывают эрозию почв и снижение плодородия. Однако все эти неприятности оказались мелкими в сравнении с тем, что произошло в последние годы.
В 1970-х годах по всем капиталистическим странам прокатился энергетический кризис, отразившийся на всей мировой экономике. Цены на нефть и природный газ фантастически возросли, а это нанесло тяжелый удар по всем энергоемким производствам. Фиксация атмосферного азота относится к этой категории. Возросшая цена на удобрения немедленно отразилась на ценах пищевых продуктов.
Проблема интенсификации сельского хозяйства стала главной проблемой, стоящей перед человечеством. И немаловажную роль в ней играет расширение производства связанного азота.
Следует сказать, что после Ф. Габера и К. Боша химики не прекратили поиски более дешевых способов фиксации атмосферного азота. Не так давно советские химики М. Е. Вольпин, Б. В. Шур, А. Б. Шилов и их сотрудники открыли новые реакции молекулярного азота с комплексными соединениями переходных металлов, таких, как железо, молибден, титан, ванадий, хром. Есть надежда с помощью этих реакций превращать азот в усваиваемые растениями соединения при низких температурах и давлениях. А это резко снизит энергетические затраты. Но этот путь не единственный. Настало время вспомнить о том, что, как бы ни было велико количество вносимого в почву фиксированного химиками азота (более 400 млн. т в год во всем мире), оно составляет менее трети от того количества азота, которое связывается в природе естественным путем, т. е. живыми микроорганизмами почвы и водоемов. Рассмотрим проблему биологической фиксации азота.
Как микроорганизмы фиксируют атмосферный азот. Земледельцы давно знали, что бобовые растения не только не нуждаются в азотных удобрениях, но и обогащают почву азотом. Этот факт был установлен до открытия самого азота. Еще в Древнем Риме рачительные хозяева использовали севообороты бобовых с другими культурами. Наши крестьяне также издавна предпочитали сеять рожь и лен на клеверищах. Но причина благодатного воздействия бобовых на плодородие оставалась загадкой. И только в XIX в. ученые установили, что азот из атмосферы связывают не сами бобовые, а микроорганизмы, образующие на их корнях клубеньки. Эти микроорганизмы - крупные палочковидные бактерии - впервые обнаружил в 1866 г. русский биолог М. Воронин, и лишь 22 года спустя М. Бейеринк сумел выделить их в чистом виде и вырастить в культуре.
Эти бактерии, получившие название Ризобиум, оказались капризными. В культуре они азот не связывали. Лишь в последнее время удалось установить, что Ризобиум начинает фиксировать азот, преобразуя его в аммиак, только при наличии определенных веществ - источников энергии - и при низком давлении кислорода. В клубеньках на корнях бобовых им кислород не страшен. Микробиологи выделили много чистых культур - штаммов Ризобиума. При этом оказалось, что Ризобиум гороха не образует клубеньки, например, у люпина и, наоборот, люпиновый не годится для гороха, но годится для бобов и чечевицы. Эти бактерии встречаются в почве относительно редко (менее 10 клеток на 1 г почвы), но бобовые стимулируют их развитие до 10 млн. на 1 г! Значит, выгода от сожительства высшего растения с бактерией обоюдная. Такие взаимоотношения, как вы знаете, называются симбиозом.
Оказалось, что клубеньковые бактерии-симбионты встречаются не только у бобовых. В последнее время открыто уже более 10 родов небобовых растений с азот- фиксирующими клубеньками на корнях. К ним относятся, например, всем известные ольха, облепиха и лох. За исключением одного рода, симбионты у них не относятся к роду Ризобиум, а более напоминают другую группу микроорганизмов - актиномицетов, известных как продуценты антибиотиков.
Однако растений, не способных получать связанный азот от симбионтов, все же несравненно больше. Откуда же они его берут? Ведь не везде же растут бобовые растения. На этот вопрос ответил в 1894 г. наш замечательный микробиолог С. H. Виноградский, разработавший изящный прием выращивания бактерий на твердой среде без азота. Мы уже упоминали об этом, когда писали о селективных средах. Обычно микробиологи выращивают колонии бактерий на поверхности желатины или агара. Но эти вещества содержат связанный азот. С. H. Виноградский использовал для своих культур гель (студень) кремневой кислоты, проще говоря, затвердевший силикатный клей с добавкой сахаров и солей. Тем самым любая колония, выросшая на этой среде, оказывалась азотфиксирующей: ведь азот она могла получать только из воздуха. Так С. Н. Виноградский открыл первую свободноживущую бактерию, способную связывать азот. Она оказалась анаэробной, живущей без кислорода, и получила название клостридиум Пастера. Род Клостридиум хорошо известен; к нему относятся, например, возбудители опаснейших заболеваний - столбняка и газовой гангрены.
С. H. Виноградский сделал еще одно важное открытие. Ему удалось показать, что происходящее в почве окисление аммиака в нитриты (соли HN02) и нитраты (соли HN03) не чисто химический процесс. Селитры в природе возникают в результате жизнедеятельности особых нитрифицирующих бактерий. Одна из них, Нитрозомонас, окисляет ион аммония в ион нитрита (N02), а другая - Нитробактер - превращает нитрит в нитрат (NO3 ). Для них реакции окисления - источник энергии. Похоже, без бактерий не обходится ни один этап превращения азота во все связанные формы.
В первом году нашего века М. Бейеринк открыл еще одного микроскопического фиксатора атмосферного азота, на этот раз аэробного, дышащего кислородом. Бактерия получила название Азотобактер. Она обогащает азотом почвы умеренного пояса. Позже выяснилось, что в кислых почвах тропиков ту же функцию выполняет другой близкий род, названный в честь М. Бейеринка - Бейеринкия.
Теперь известно немало свободноживущих микроорганизмов - фиксаторов атмосферного азота. Пожалуй, наиболее интересна из них бактерия Клебсиелла. Это близкий родственник кишечной палочки Эшерихии коли, обитающей в кишечнике каждого из нас. Кишечная палочка - один из наиболее изученных организмов на Земле. Поэтому близкая к ней Клебсиелла оказала неоценимую услугу в изучении тонких деталей механизма биологической фиксации азота.
М. Бейеринк открыл еще целую группу азотфиксаторов, так называемые сине-зеленые водоросли. Строго говоря, это не водоросли, а одна из ветвей бактерий. Правильнее их называть цианобактериями или цианофитами.
В нитчатых колониях цианобактерий встречаются своеобразные клетки, практически не содержащие фото- синтезирующего пигмента. Они прозрачны и имеют толстую двухслойную оболочку - гетероцисты. Назначение гетероцист долгое время оставалось неясным, однако ученые подметили, что связывают азот только те сине-зеленые, которые образуют эти специализированные клетки. Согласно последним данным плодородие почвы обеспечивают наряду с клубеньковыми бактериями и цианобактерии, причем роль последних иногда оказывается важнее.
Некоторые цианобактерии также вступают в симбиоз с другими организмами. Вы знаете, что лишайник - симбиоз гриба и водоросли. У многих лишайников эта "водоросль" сине-зеленая, способная фиксировать азот. Поэтому они могут расти даже на оконном стекле.
Другие цианобактерии - симбионты древних тропических растений - цикадовых (тех, что неправильно называют саговыми пальмами). Агрохимиков давно занимал интересный факт. Рисовые заливные поля Южной Азии при чрезвычайно интенсивной системе хозяйства не снижают плодородия, хотя о селитре там и не слыхали. Оказалось, что рис снабжают азотом сине- зеленые, в первую очередь симбионты крошечного водяного папоротника Азоллы. Азоллу во Вьетнаме усиленно изучают; это растение, возможно, будет компонентом искусственных экологических циклов в космических кораблях. Во всяком случае, оно уже побывало в космосе вместе с В. В. Горбатко и Фам Туаном.
Итак, азотфиксаторов, как симбиотических, так и свободноживущих, к настоящему времени описано уже немало. Но все они относятся к прокариотам - организмам без оформленного ядра. Эукариоты - высшие растения, грибы, животные усваивать атмосферный азот оказались неспособными.
Выдающийся вклад в разгадку тайны фиксации атмосферного азота внесли русские и советские ученые. Еще в 1920-х годах С. П. Костычев доказал, что в основе биологического связывания азота (N2) лежит процесс восстановления его "активированным водородом органического вещества". Иными словами, в живых клетках азотфиксаторов осуществляется тот же процесс, что и в установках Габера - Боша, но при низкой температуре и атмосферном давлении!
В чем тут разгадка? Вспомните, что и 500°С температуры, и 300 атмосфер давления еще недостаточны для синтеза аммиака по Габеру и приходится прибегать к катализатору - веществу, ускоряющему химическую реакцию.
С. Н. Виноградский в 1932 г. пришел к выводу, что реакция биологической фиксации азота ускоряется настолько, что становится возможной и выгодной в условиях, совместимых с жизнью, особым ферментом, который он назвал нитрогеназой.
К середине 1950-х годов было доказано, что все микроорганизмы, способные фиксировать азот атмосферы, содержат фермент нитрогеназу, который катализирует восстановление N2 в конечном итоге до NH4+. С этого момента основные усилия ученых сконцентрировались на изучении строения, механизма действия, регуляции активности и регуляции биосинтеза нитрогеназы.
Волшебная нитрогеназа. Фермент нитрогеназа - очень сложный белок. Он слагается из двух частей, получивших название компонент I и II. Компонент I, имеющий молекулярную массу 220 000, содержит от 28 до 34 атомов железа и 2 атома молибдена, поэтому его называют FеМо-белком. Компонент II меньше (молекулярная масса 60 000) и содержит 4 атома железа. Его называют Fe-белком. Оба белка содержат также большое количество серы в виде сульфидов. Эти неорганические добавки наводят на размышления. Вспомним, что в реакциях связывания азота, изучаемых М. Е. Вольпиным и А. Б. Шиловым, участвуют комплексные соединения металлов, в том числе железа и молибдена. Не пытаются ли химики-биоорганики заново создать механизм, уже реализованный природой в живых клетках азотфиксаторов?
Компоненты I и II также сложные образования. Они состоят из более мелких субъединиц, причем каждая субъединица сложена одной полипептидной цепью и кодируется своим геном. FеМо-белок состоит из двух субъединиц одного сорта (их назвали α-субъединицами) и двух - другого (β-субъединицы). Структуру его можно написать сокращенно α2β2. Fe-белок проще, его структура ?2, т. е. он состоит из двух одинаковых цепочек аминокислот (рис. 44).
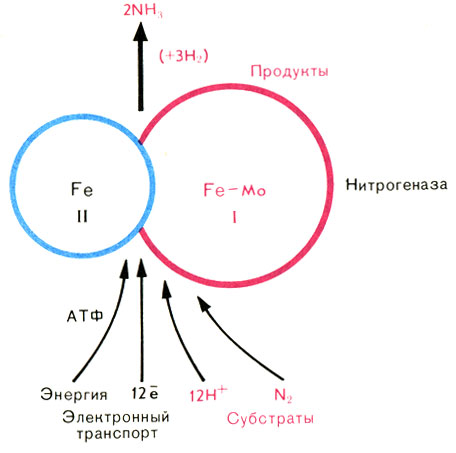
Рис. 44. Схема работы нитрогеназы
Замечательно, что нитрогеназы, изолированные из любого микроорганизма, фиксирующего азот атмосферы, построены практически одинаково. Субъединицы этих белков довольно сходны и по аминокислотной последовательности. Не удивительно поэтому, что активная нитрогеназа может быть построена из компонента I, выделенного из одного микроорганизма (например, Клебсиеллы), и компонента II, полученного из совсем другого источника (например, азотобактера).
Получение таких молекул-химер свидетельствует о многом. В первую очередь о том, что механизм биологической фиксации азота очень консервативен и возник в глубокой древности, когда первичные организмы исчерпали весь связанный азот на поверхности Земли и столкнулись с проблемой азотного голодания. С тех пор этот механизм в своих общих чертах практически не менялся.
Собственно восстановлением азота в аммиак занимается FеМо-белок. Расчеты показывают, что эта реакция должна идти в несколько стадий с образованием промежуточных продуктов, нам еще не известных. На схеме в качестве промежуточного соединения показан гидрид азота - это вполне вероятно, но еще не доказано.
Заметьте также, что, восстанавливая азот, FeMo-бeлок отдает электроны ионам водорода (протонам), превращая их в газообразный водород. Эта важная побочная реакция, катализируемая нитрогеназой, также может найти практическое применение. Ведь водород называют топливом будущего.
Задача Fe-белка, по-видимому, сводится к тому, чтобы поставлять электроны FeMo-белку. Поэтому компонент II часто называют белком-восстановителем или редуктазой.
Нитрогеназа способна катализировать реакцию превращения (восстановления) ацетилена в этилен:
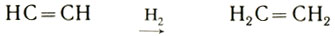
Это объясняется, видимо, сходством связей между атомами углерода в молекуле ацетилена и атомами азота в его молекуле
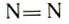
Вряд ли в природе этот процесс происходит, но для определения активности фермента реакция восстановления ацетилена оказалась очень удобной. Ацетилен хорошо растворяется в воде, а этилен плохо, поэтому легко можно отделить продукт реакции от исходного вещества и определить его количество. Теперь такие измерения проводятся даже в полевых условиях.
Как и все ферменты, нитрогеназа, несмотря на свои чудесные свойства, не может совершить невозможного: для биологического синтеза NH3 из N2 требуется энергия, львиная доля которой идет на разрыв связей в молекуле азота. Эти энергетические затраты покрываются за счет гидролиза универсального источника энергии клетки - аденозинтрифосфата (АТФ). К этой важной стороне мы еще вернемся.
Кроме нитрогеназы, в биологическом синтезе аммиака участвуют и другие белки. Все они наряду с полипептидами, слагающими FeMo- и Fe-белки, кодируются определенными генами. Эти гены называют nif-генами (от первых букв слов нитоген-фиксация). Мы уже упоминали, что способностью связывать азот обладает и близкий родственник кишечной палочки - Клебсиелла. Ее генетический аппарат детально изучен. У Клебсиеллы оказалось 17nif-генов. Они объединены в 7 групп, именуемых nif-оперонами. Продукт деятельности каждого оперона - соответствующая иРНК, на которой синтезируется белок. nif-Опероны разбросаны по единственной хромосоме бактерии; между ними встроены гены, не имеющие отношения к фиксации азота.
Функции многих продуктов nif-генов сейчас известны. Так, гены nif К и nif D кодируют полипептидные цепи белков - предшественников субъединиц FeMo-белка. Гены nif В, nif N и nif Е кодируют белки, которые превращают эти предшественники в нормальные α- и β-субъединицы компонента I. Белки - продукты генов nif А и nif L - заняты регуляцией активности нитрогеназы в клетке и т. д. Процесс регуляции активности nif-генов очень сложный. Так, у Клебсиеллы найдены еще три гена, не входящие в состав nif-оперона (их назвали ntr А, В и С), продукты которых регулируют активность nif А- и nif L-белков. Иными словами, они работают как регуляторы активности регуляторов.
Генетики научились "вырезать" отдельные nif-гены или целые nif-опероны из хромосомы Клебсиеллы, а также у некоторых других микроорганизмов и переносить их в хромосомы других бактерий. В клетках кишечной палочки (которая неспособна фиксировать N2) ученым даже удалось заставить на короткое время заработать нитрогеназу Клебсиеллы. А в клетках азотобактера нитрогеназа Клебсиеллы чувствовала себя совсем хорошо и работала в аэробных условиях (напомним, что сама Клебсиелла - анаэроб). Правда, перенос всех 17 nif-генов из Клебсиеллы в клетки дрожжей - простейших эукариотов - не привел к синтезу аммиака.
Располагая отдельными nif-генами Клебсиеллы, генетики сумели также определить, как эти гены организованы в хромосомах других микроорганизмов, фиксирующих азот атмосферы. При этом обнаружился интересный и практически важный факт: у Ризобиум - микроорганизмов, населяющих клубеньки на корнях бобовых растений, - nif-опероны находятся не в хромосоме, а в составе специальных крупных плазмид. В принципе можно выделять эти плазмиды и вставлять в клетки микроорганизмов, не способных к фиксации азота!
Как перенести ген в клетку растения. Возникает вопрос: если известен белок, отвечающий за фиксацию азота атмосферы, если генетики получили гены, кодирующие составляющие этого белка, то почему не перенести эти гены в клетки зеленых растений?
Прежде чем ответить на этот вопрос, мы должны задать другой вопрос: а существуют ли векторы - плазмиды или вирусы, которые позволят перенести чужеродную ДНК в клетки растений? Ведь растительная клетка и по структуре клеточных стенок, и по своему внутреннему устройству так сильно отличается от бактериальной, что для нее вряд ли подойдут известные бактериальные векторы, о которых мы рассказали в предшествующих главах. Если же вирусов или плазмид, пригодных для переноса генов в растительную клетку, не найдется, сам вопрос о генной инженерии у растений отпадает.
Но и здесь все складывается, казалось бы, как нельзя лучше. Оказалось, что бактерии Агробактериум тумефациенс, обладающие давно известным свойством вызывать опухоли (так называемые галлы) у многих растений, содержат плазмиды, которые специально приспособлены к переносу генов из бактериальной в растительную клетку. Именно в этих плазмидах закодированы белки, вызывающие трансформацию нормальных клеток растений в раковые. Их называют Ti-плазмидами (Ti - tumor induciug), индуцирующими опухоли.
Обычно нормальное развитие растительной клетки регулируется специальными гормонами, так же как и развитие животной клетки. О гормонах роста животных мы уже говорили раньше. Естественно, фитогормоны имеют совсем другое химическое строение, чем соматотропин, соматостатин и другие гормоны животных. Однако функции их сходны: и те и другие стимулируют рост, развитие и специализацию одних клеток и подавляют те же процессы у других. Белки, закодированные в Ti-плазмидах, нарушают такую гормональную регуляцию, и клетки растений начинают расти бесконтрольно. Ti-плазмиды имеют очень большие размеры - около 200 тыс. пар оснований. Однако они содержат сравнительно небольшую область (13 тыс. пар оснований) так называемой Т-ДНК, которая встраивается в хромосому растительной клетки, стабильно сохраняется и функционирует в ней. Таким образом, гены, встроенные в Т-ДНК, хотя и имеют бактериальное происхождение, но уже снабжены всеми необходимыми "сигналами", обеспечивающими их работу в растительной клетке. Если встроить nif-гены в Т-ДНК Ti-плазмиды, то теоретически можно получить на растениях полезные галлы, которые будут фиксировать азот атмосферы. Такие галлы будут напоминать клубеньки на корнях бобовых растений, которые, кстати, также относятся к растительным опухолям - галлам (рис. 45).
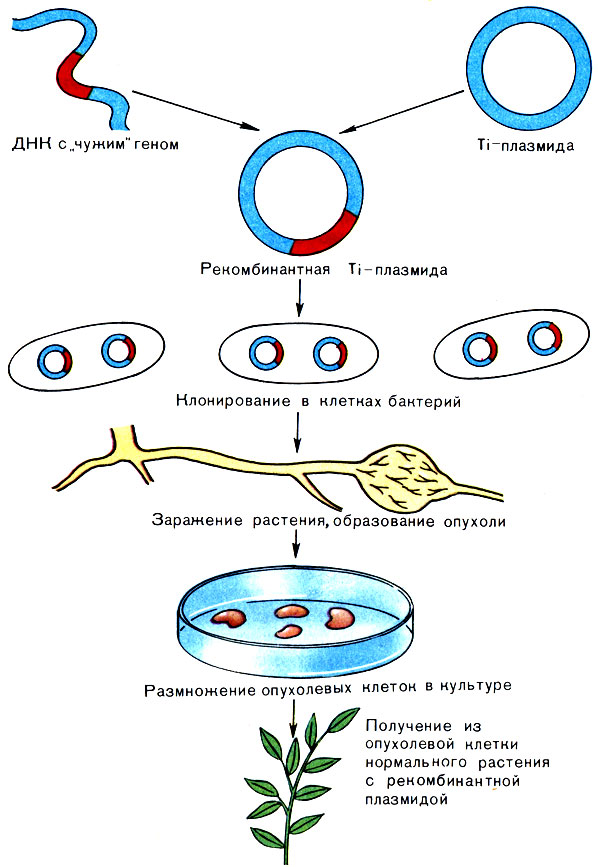
Рис. 45. Схема получения рекомбинантного высшего растения с помощью Ti-плазмиды. Здесь используется свойство некоторых опухолевых клеток растения образовывать нормальные растения
Из Ti-плазмиды генные инженеры уже создали удобные векторные системы для переноса чужеродных генов сначала в клетки Агробактериум, а затем с помощью этой бактерии (и второй специально сконструированной плазмиды, заранее помещенной в клетки Агробактериум) включили чужеродные гены в геном растения. Такие векторы называют бинарными (двойными), потому что они работают в паре - показано на рисунке. Обратите внимание на то, что вектор, в который встраивается чужеродный ген, - это типичный челночный вектор, т. е. он может реплицироваться как в бактериальной, так и в растительной клетке.
Бинарная векторная система с успехом использована для переноса в клетки растений признака устойчивости к антибиотику канамицину (для многих растений он ядовит). С ее помощью получены светящиеся листья табака после того, как в геном этого растения включили ген белка люциферазы, выделенный из светлячков. Ген люциферазы в генетической инженерии растений надеются использовать как маркер, подобно тому как ген 8-галактозидазы (помните голубые колонии?) используют в генной инженерии микроорганизмов.
Существуют и другие способы направленного переноса в растительную клетку чужеродной ДНК. Мы писали, что недавно были открыты ДНК-содержащие вирусы растений. Это открытие сначала показалось удивительным: ведь большинство растительных вирусов содержат не ДНК, а РНК. Если генетическим путем превратить эти вирусы в непатогенные (т. е. сделать их безвредными) для растения, то они могут оказаться подходящими векторами для nif-генов.
Что мешает создать азотфиксирующее растение? К сожалению, на пути конструирования новых видов растений, фиксирующих азот атмосферы без помощи микроорганизмов, стоят очень серьезные трудности. Первая трудность состоит в том, что в растительной и бактериальной клетках действуют совершенно различные механизмы регуляции активности генов. Иными словами, процессы транскрипции (синтез РНК на ДНК) и трансляции (синтез белка) у прокариот и эукариот управляются различными сигнальными последовательностями генов и различными белками. Выход здесь подсказывает изучение генома хлоропластов. Как вы знаете, хлоропласты - это обособленные органеллы растительных клеток, осуществляющие процесс фотосинтеза. Хлоропласты имеют собственный геном достаточно большого размера (от 80 до 200 тыс. пар оснований). Есть обоснованная гипотеза о том, что хлоропласты происходят от симбиотических микроорганизмов - фотосинтетиков (ближе всего к ним сине-зеленые, цианофиты). Генная инженерия эту гипотезу подтвердила. Структура генов, составляющих этот геном, хорошо изучена у многих растений. А для табака известна нуклеотидная последовательность всего генома хлоропластов (около 150 тыс. пар оснований). Анализируя строение этих генов, молекулярные биологи обнаружили в них те же сигналы транскрипции (промоторы и терминаторы) и трансляции, что и у генов бактерий. Более того, хлоропластный ген очень важного фермента - карбоксилазы (о котором мы подробнее расскажем позже) - активно работал после того, как его перенесли в клетки кишечной палочки.
Следовательно, хлоропласты - это прекрасное помещение для nif- и ntr-генов бактерий. Кстати, генные инженеры сейчас интенсивно работают над конструированием из хлоропластной ДНК векторов, которые и позволят переносить чужеродные (например, бактериальные) гены непосредственно в хлоропласты. Здесь, правда, возникает новая трудность: ведь в хлоропластах в результате фотосинтеза возникает свободный кислород, а кислород и работающая нитрогеназа несовместимы.
О другой проблеме мы уже рассказывали: биологическая фиксация азота подобно химической требует огромных энергетических затрат. В клетке эти расходы в конечном итоге покрываются за счет гидролиза АТФ. При отщеплении от АТФ одной молекулы Н3Р04 образуется адениндифосфат и выделяется энергия, потребляемая клеткой. Так, Клебсиелла расходует по разным оценкам от 12-14 до 29 молекул АТФ на превращение одной молекулы N2 в ионы аммония. А если учесть, что при работе нитрогеназы ее компонент II (Fe-белок) получает электроны от таких биологических восстановителей, как ферродоксин и флаводоксин, то на биологическую фиксацию одного моля N2 этим организмом расходуется до 40 эквивалентов АТФ. Значит, если в клетку растения или какого-то другого организма, не приспособленного природой для фиксации азота атмосферы, просто ввести нитрогеназу и заставить ее работать, то это мгновенно исказит ее энергетический обмен, и клетка погибнет от аденозинтрифосфатного голода. Клетка попросту надорвется, как человек, под непосильным грузом.
Еще одна, пожалуй, более серьезная трудность заключена в свойствах самой нитрогеназы. Если этот фермент изолировать из фиксирующего азот микроорганизма, то он мгновенно инактивируется, "отравляется" кислородом воздуха. Причем водород отравляет нитрогеназу необратимо, т. е. если фермент вновь поместить в бескислородную среду, то он остается неактивным. Из этого следует, что процесс биологической фиксации азота возник, когда земная атмосфера еще не содержала кислорода. Населявшие Землю микроорганизмы были анаэробами и получали энергию за счет реакций, схожих с современным брожением, а фотосинтезирующие бактерии усваивали сероводород. Со временем сине-зеленые выработали способность при помощи солнечного света расщеплять воду и получать углеводы из образующегося при этом водорода и углекислого газа (С02). Запасы водорода в воде оказались неисчерпаемыми, но при этом выделялся вредный побочный продукт... кислород, абсолютно ядовитый для всех тогда живущих существ! Это потом кислород стал живительным газом, когда возникло кислородное дыхание. Но все черты фиксации азота менять было уже поздно. У тех организмов, которые возникли позже, т. е. у животных и растений, этот процесс вообще не возник, а микроорганизмы-азотфиксаторы выработали сложные механизмы, защищающие нитрогеназу от кислородного отравления. Следовательно, если мы перенесем nif-гены в клетки, которые не умеют защищать нитрогеназу от кислорода, то в лучшем случае мы получим неактивный фермент, а в большинстве случаев такая клетка быстро прекратит синтез ненужного ей белка.
И наконец, еще одна трудность, с которой встретились генетики, конструирующие новые фиксирующие азот организмы, состоит в том, что ионы аммония, образующиеся при восстановлении азота, должны сразу же использоваться другими ферментативными системами для синтеза аминокислот. Если же они накапливаются в клетке в слишком больших количествах, то биосинтез нитрогеназы (правда, на этот раз обратимо) подавляется. Этот механизм позволяет клеткам многих фиксирующих азот микроорганизмов связывать ровно столько атмосферного азота, сколько им необходимо для внутренних нужд. Продукт реакции, накопленный в достаточном количестве, быстро останавливает ее; поэтому ионов аммония в клетке всегда столько, сколько необходимо и достаточно. Ясно, что для сверхпродукции "связанного азота" клетки с такой системой регуляции не годятся. Эту последнюю трудность удалось преодолеть сравнительно легко.
Советский генетик С. В. Шестаков получил мутанты цианобактерий, которые выбрасывают все избыточные ионы аммония из цитоплазмы клеток в среду. Кроме того, у этих мутантов нарушена система, ответственная за подавление биосинтеза нитрогеназы ионами аммония. О получении подобных мутантов азотбактера сообщили недавно американские генетики. Такие мутантные микроорганизмы уже сами по себе могут оказаться очень полезными как сверхпродуценты асиммилируемого азота. Кроме того, они помогут выявить тот ген, который необходимо выключать, чтобы клетка могла бесконтрольно превращать азот в ионы аммония.
Значительно более сложными оказались проблемы энергетики фиксации азота и защиты нитрогеназы от отравления кислородом. Тем более что эти процессы противоречиво связаны. Чтобы получить достаточное количество АТФ для энергоемкого процесса фиксации азота, клетке надо дышать кислородом (бескислородный синтез АТФ - брожение - дает энергию примерно в 18 раз меньше). Но тот же кислород отравит нитрогеназу. Вставлять nif-гены в клетку с кислородным дыханием - все равно что разводить рыб на суше.
Каким же путем все-таки можно снизить расход энергии при превращении N2 в NH3, катализируемом нитрогеназой? Одно направление работ подсказывает рассмотренный нами механизм работы этого фермента. Давайте еще раз вернемся к рисунку. Как мы видим, значительная доля электронов (а следовательно, и значительная доля энергетических ресурсов в виде молекул АТФ) расходуется на восстановление ионов водорода - протонов (H+) до молекул водорода. В среднем нитрогеназа расходует две молекулы АТФ на перенос одного электрона. Эта побочная реакция с точки зрения самого процесса фиксации азота есть не что иное, как излишняя трата энергии. А что если образующийся молекулярный водород снова превратить в протоны и электроны: ведь электроны вновь могут быть использованы в нитрогеназной реакции? Клетка осуществляет такое превращение водорода с помощью фермента гидрогеназы. Этот фермент, а также ряд других белков, способствующих превращению газообразного водорода в протоны и электроны, закодированы в так называемых hup-генах. Оказывается, что некоторые дикие штаммы Ризобиум уже содержат hup-гены, и урожай бобовых, живующих в симбиозе с такими бактериями, всегда намного выше, чем у растений, в клубеньках которых бактерии обычные.
Таким образом, при конструировании новых фиксирующих азот организмов генетики предполагают наряду с nif-генами вводить в клетки hup-гены (гены "захвата" молекулярного водорода). Источником таких генов будут скорее всего легкодоступные бактерии из рода Псевдомонас, способные расщеплять нефтепродукты, у которых hup-гены находятся в составе специальных плазмид (т. е. уже от природы встроены в векторы).
Другой, не менее важный путь преодоления "энергетического кризиса", связанного с введением в организм nif-генов, лежит в направленном совершенствовании энергетики этого организма.
Известно, что для всех зеленых растений, а также для многих микроорганизмов (сине-зеленых, например) основным источником энергии служит солнечный свет. В результате процесса фотосинтеза с помощью молекул пигмента хлорофилла, главного участника преобразования световой энергии в химическую, из воды и углекислого газа образуются углеводы и молекулярный кислород. Благодаря фотосинтезу в этих организмах идет также образование аденозинтрифосфата и других переносчиков энергии.
Оказывается, эффективность фотосинтетической фиксации С02 также можно повысить генетическим путем. Ясно, что это перспективно не только для фиксации азота, но и для повышения общей продуктивности растения. Дело в том, что фермент карбоксилаза - ключевой катализатор фиксации углекислого газа - так же, как и нитрогеназа, наряду с основной полезной реакцией (ведущей к синтезу источников углеводов) катализирует побочную и бесполезную с точки зрения синтеза источников энергии реакцию, которая в конечном итоге приводит вновь к освобождению С02. Эту реакцию можно подавить, если, например, выращивать растение в атмосфере, обогащенной углекислым газом. Однако изменять состав атмосферы, в которой растут сельскохозяйственные растения, слишком дорого (это можно делать только в теплицах). Генетики пошли другим путем. Они получили такие мутантные формы фермента карбоксилазы, которые потеряли способность катализировать побочную реакцию и тем самым направили фиксируемый углекислый газ только на синтез углеводов.
Очень интересная возможность в повышении эффективности использования продуктов фотосинтеза заключена в усовершенствовании ферментативных систем "метаболизма" воды. Молекулы воды при фотосинтезе служат источником электронов, используемых для образования АТФ. Недавно у цианобактерий удалось найти гены (так называемые lit-гены), в которых закодированы белки, расщепляющие молекулы воды. Генетики надеются, увеличивая число таких генов в клетках фотосинтетиков, существенно улучшить их энергетику.
Чему нас могут научить бактерии. Теперь давайте посмотрим, как обстоит дело с защитой нитрогеназы от кислорода у разных фиксирующих азот атмосферы организмов. У таких бактерий, как Клебсиелла, этой проблемы вообще не существует. Ведь Клебсиелла усваивает атмосферный азот только тогда, когда она живет в анаэробных (бескислородных) условиях. Она, как говорят микробиологи, факультативный анаэроб. В присутствии О2 эти бактерии могут расти только на готовых источниках азота. Их нитрогеназа при этом не только не работает, но и не синтезируется. Да и в знаменитом опыте, когда nif-гены из Клебсиеллы заработали в кишечной палочке, эта бактерия фиксировала азот тоже только в анаэробных условиях. Ведь в нашем кишечнике она живет без кислорода, получая энергию благодаря сбраживанию углеводов. Таким образом, Клебсиелла не может быть использована для спасения нитрогеназы от кислорода. Азотфиксатор из рода Клостридиум также не может помочь: клостридии - облигатные (обязательные) анаэробы, гибнущие в кислородной среде.
Другое дело цианобактерии. Как вы уже знаете, у цианобактерий, фиксирующих азот атмосферы (например, у анабены, живущей в симбиозе с азоллой - мелким водяным папоротником), наряду с нормальными пигментированными клетками (ведь цианобактерии - это фотосинтетики) имеются присоединенные к ним дополнительные клетки, названные гетероцистами. Гетероцисты возникают у анабены только тогда, когда у них нет для питания другого источника азота, кроме атмосферного. Если кормить ее солями аммония или селитрой, то гетероцисты исчезают. У анабены, фиксирующей азот атмосферы, вся нитрогеназа содержится в гетероцистах; причем клеточные стенки гетероцистов устроены так, что доступ кислороду в них закрыт. По последним данным, в гетероцистах то небольшое количество кислорода, которое вместе с азотом проникает через оболочки, активно связывается особыми реакциями. Все же необходимые для работы нитрогеназы источники энергии поступают в гетероцисты из нормальных соседних фотосинтезирующих клеток. Таким образом, гетероцисты - это не что иное, как специализированные фабрики азотистого питания, сырьем для которых служит азот атмосферы, а энергетическим источником - солнечный свет.
Эффективность гетероцист как защитного средства демонстрируется простым опытом: связывание азота идет и в бесклеточных экстрактах из сине-зеленых, но только в бескислородной среде. При 5% кислорода нитрогеназа, не защищенная гетероцистами, отравляется за считанные минуты, а ведь в воздухе кислорода в 4 раза больше. Даже 0,1% кислорода заметно подавляет синтез иона аммония.
Любопытно, что ископаемые остатки сине-зеленых, содержащих гетероцисты, обнаружены в отложениях возрастом около 2,2 млрд. лет. Более ранние отпечатки цианобактерий гетероцист не имеют. Значит, кислород стал поступать в атмосферу Земли немногим ранее 2 млрд. лет назад; следовательно, и кислородное дыхание не может быть старше. Человек, попавший в такую атмосферу, задохнулся бы мгновенно. Значит, если вставлять азотфиксирующие гены в хлоропласты, необходимо превратить эти органеллы во что-то вроде гетероцист, но внутриклеточных симбионтов высшего растения. У таких растений будут и нормальные хлоропласты, и новые органеллы - "нитропласты".
Замечательная система защиты нитрогеназы выработалась у Ризобиум. Напомним, что этот важнейший фиксатор атмосферного азота живет в симбиозе с бобовыми растениями. Ризобиум, проникая в клетки корней бобовых, вызывает на них образование клубеньков. В клубеньках Ризобиум разрастается в своеобразные колонии клеток, окруженные плотным слоем клеток растения. Вот эти растительные клетки и вырабатывают белок, защищающий нитрогеназу от кислорода. Интересно, что этот белок оказался аналогом гемоглобина крови - белка - переносчика кислорода у человека и животных. Поэтому он был назван леггемоглобином (лег от английского legume - бобовые). Гемоглобин крови состоит из двух частей: белковой (глобина) и железопорфириновой (гема), которая собственно и связывает кислород. Такие же две части синтезируются клетками растений, а железопорфириновая (гем) - клетками Ризобиум. Таким образом, растительные клубеньковые клетки растения снабжают клетки Ризобиум глобином, который, соединяясь в них с гемом, образует леггемоглобин, связывающий главного "врага" нитрогеназы - молекулярный кислород. Поэтому скопления Ризобиум в клубеньках всегда окрашены в красный цвет. Из клеток растения в Ризобиум поступают также источники энергии в виде продуктов фотосинтеза (они образуются в листьях растения и затем транспортируются в его корневую систему), а Ризобиум питает растение фиксированным азотом атмосферы. Так выглядит симбиоз растения и микроорганизма на биохимическом уровне.
Многому можно научиться у азотобактера. Он живет не только вне растений, но и в кислородсодержащей среде. Тем не менее его нитрогеназа исправно работает. Происходит это потому, что азотобактер очень интенсивно дышит и быстро расходует весь кислород, который проникает в его клетки. Но даже если затруднить дыхание азотобактера, то он не сразу прекращает существование. Его клетки начинают вырабатывать так называемый Fe-S-белок, т. е. белок, содержащий железо и серу. Достаточно одной молекуле такого белка связаться с нитрогеназой, чтобы обезопасить ее от кислорода. В комплексе с Fe-S-белком нитрогеназа практически не работает, но зато стоит убрать кислород, и этот белок как активность фермента полностью восстанавливается (вспомним, что незащищенную нитрогеназу кислород отравляет необратимо). Сейчас генетики сумели разобраться, в каком из генов азотобактера закодирован Fe-S-белок. Этот ген также будет необходим при создании новых организмов, фиксирующих азот атмосферы.
Известно далеко не все о том, какие еще существуют выработанные природой способы защиты нитрогеназы от кислорода. Так, клубеньковые микроорганизмы, живущие в симбиозе с ольхой, обходятся без леггемоглобина. Ясно, что какое-то противоядие от кислорода у них есть. Добавим, что пока известны далеко не все биохимические фиксаторы азота, в арсенале природы наверняка имеется их немало.
Теперь, кажется, известно, как спланировать работу по созданию зеленого растения, фиксирующего атмосферный азот без помощи микроорганизмов. Для этого нужно:
- выделить гены азотофиксации из любого фиксирующего азота атмосферы организма, который заранее превращен в сверхпродуцент NH4 (т. е. организм с де репрессированным синтезом нитрогеназы);
- перенести их стандартными методами генетической инженерии в Т-ДНК в район Ti-плазмиды;
- перенести в эти же плазмиды гены, кодирующие синтез леггемоглобина, который защитит. нитрогеназу от кислорода;
- включить в эти плазмиды гены энергетического обеспечения работы нитрогеназы (hup, lit, а также гены "улучшенной" карбоксилазы);
- трансформировать этими рекомбинантными Ti- плазмидами клетки растения.
К сожалению, время для таких прямых опытов еще не пришло: мы слишком мало знаем о физиологии и генетическом аппарате растительных клеток, чтобы рассчитывать на быстрый успех.
Но ведь проблема увеличения пищевых ресурсов требует немедленного разрешения: уже сейчас сотни миллионов людей в слаборазвитых странах страдают от постоянного недостатка белковых продуктов, а по данным ООН на земном шаре каждые 4 секунды от недоедания умирает один ребенок. Поэтому ученые, изучающие биологическую фиксацию азота, направляют усилия на решение более реальных задач.
Во-первых, это конструирование новых фиксирующих азот микроорганизмов-фотосинтетиков, которые усваивают атмосферный азот благодаря солнечной энергии. Кроме того, ученые научились превращать их в такие формы, которые выбрасывают все избыточные азотистые соединения в среду. Следовательно, остается создать более продуктивные по синтезу аммиака штаммы этих микроорганизмов.
Основное требование к новым формам азотфиксаторов - более интенсивная фиксация азота атмосферы при тех же (или даже меньших) затратах энергии. Дикие клубеньковые бактерии можно улучшить, как человек улучшил грибок - продуцент пенициллина, заставив его синтезировать антибиотик в тысячи раз активнее. Вы уже познакомились с тем, каким образом генетики решают подобные задачи: это освобождение нитрогеназы от зависимости концентрации ионов аммония в клетке, введение в клетку генов гидрогеназы, увеличение фотосинтетических возможностей самого растения и т. д. Правда, в реальных полевых условиях "новички" должны сосуществовать с огромным миром микроорганизмов, населяющих почву. А главное, они должны выдерживать борьбу за существование и побеждать в этой борьбе со своими непосредственными родственниками - клубеньковыми бактериями, которые привыкли жить в симбиозе с растением. Это сложная проблема: ведь высшие культурные растения, как правило, оказываются "побитыми" дикими сорняками. Вот почему ученые, создавая новые формы микроорганизмов, сразу отбирают те из них, которые способны выдержать конкуренцию с хозяевами почвы. В последние годы микробиологи и генетики добились серьезных успехов в повышении урожайности соевых бобов, сконструировав для них новые штаммы Ризобиум. Соя, как известно, - один из основных поставщиков полноценного белка сейчас и в ближайшем будущем.
Решая проблему "азотного голода", генетики не только улучшают известные виды азотфиксирующих симбионтов, но и работают над созданием новых почвенных микроорганизмов. Дело в том, что, кроме клубеньковых бактерий, живущих на корнях лишь немногих растений, в ризосфере (так называют корневую систему с прилегающей к ней почвой) любого растения обитает богатейший и специально приспособленный к ней мир микроорганизмов. Некоторые из них живут непосредственно на корнях растений, другие - возле них. Ризосферные микробы питаются в значительной мере выделениями корней, но и сами снабжают растения полезными продуктами своей жизнедеятельности.
К сожалению, в ризосферной микрофлоре очень мало видов, фиксирующих атмосферный азот. Свободно живущие азотфиксаторы, например азотобактер, почему-то предпочитают жить вне ризосферы. Микробиологи и генетики пытаются сейчас выяснить этот вопрос. Какие особенности генетического аппарата ризосферных бактерий заставляют их из поколения в поколение селиться на корнях высших растений? Кое-что ясно уже сейчас. В состав клеточной стенки бактерий входят специальные сложные углеводы - полисахариды с составом, характерным для каждого определенного вида. Эти специфичные для вида вещества и помогают бактериям "узнать" на стенке клеток, слагающих оболочку корня, специальные места (рецепторы) и приклеиться к ним. Такое взаимное "узнавание" обязательно происходит и у клубеньковых бактерий, и корней бобовых, прежде чем бактерии проникнут внутрь корня. Все это удивительно напоминает "узнавание" антителом своего антигена.
У клубеньковых бактерий гены "узнавания" недавно были найдены в составе плазмид. Это открытие трудно переоценить. Ведь с помощью таких генов можно "приручить" к растениям мощные фиксаторы азота, которые чуждаются ризосферы, или приучить ризосферных азотфиксаторов (например, азоспирилл) к другому хозяину. На каждом пути перед исследователями встают трудности.
Ризосферные бактерии привыкли жить вместе с другими обитателями корневой системы; поэтому им, наверное, легче выстоять в борьбе за существование при смене хозяина. В сельском хозяйстве давно применяется препарат "нитрагин" - масса подсушенных клубеньковых бактерий, которой заражают семена бобовых перед посевом. Ученые надеются на основе новых форм азотобактера, "прирученного" к специфическим условиям ризосферы, или новых форм азоспирилл создать эффективные биологические азотные удобрения - новые "азобактерин" и "спириллин".
Другой путь: среди постоянных жителей ризосферы полезных сельскохозяйственных растений, например пшеницы, найти такие ризосферные микроорганизмы, которые легко превратить в азотфиксаторов. Для этого нужно перенести в них nif-гены и другие гены, обеспечивающие энергетику работы нитрогеназы и защиту этого фермента от кислорода.
Оптимисты считали, что такие формы ризосферных микроорганизмов будут получены к 1985 г., пессимисты отодвигали этот срок до 1990 г. Как видим, надежды возлагались на ближайшее будущее. В печати появилось сообщение, что австралийским ученым удалось вставить бактериальные гены в клетки томатов, и теперь растение "может брать необходимый для жизни азот непосредственно из воздуха, не нуждаясь более в минеральных удобрениях". Увы, нитрогеназа в клетках томата будет бесполезным грузом.
Наш рассказ будет неполным, если не упомянуть еще об одной, на первый взгляд фантастической идее - создать азотфиксирующих животных! Казалось бы, невероятно. Однако это более реально, чем азотфиксирующие томаты. Речь снова идет о микроорганизмах, только живущих в качестве симбионтов и комменсалов (нахлебников) в желудочно-кишечном тракте. То небольшое количество воздуха, которое в нем имеется, практически не содержит кислорода в отличие от плазмы клеток. Если создать азотфиксирующих энтеробактерий (а это нетрудно, вспомним про ближайшую родственницу кишечной палочки - Клебсиеллу) и придать им способность сосуществовать с нормальной микрофлорой кишечника, то, фиксируя молекулярный азот, такие бактерии могли бы стать полезным источником азотного питания животных. А может быть, и людей? В научной литературе встречались непроверенные спорные сообщения, что в кишечниках аборигенных обитателей влажного тропического леса, пища которых содержит недостаточно белков, имеются азотфиксирующие бактерии.
Приведем и достоверный факт. Южные насекомые - термиты (их называют "белыми муравьями", хотя они близки к тараканам) - могут неограниченное время питаться одной клетчаткой (например, фильтровальной бумагой). Сами термиты клетчатку (целлюлозу) не переваривают, за них это делают микроорганизмы-симбионты, обитающие в их кишечниках. Среди них есть и азотфиксаторы: ведь клетчатка азота не содержит. В конечном счете термиты питаются не клетчаткой, а своими симбионтами. Но стоит термитов подержать при повышенном давлении кислорода, как он, проникнув в пищеварительный тракт, отравит нитрогеназы симбионтов, погибнет вся микрофлора кишечника, и термитам одной клетчатки будет недостаточно. Стерильным термитам нужны аминокислоты, на "диете" из одной фильтровальной бумаги они погибнут с голоду.
Аналогичные симбионты, выведенные для домашних животных, решили бы проблему кормов самым радикальным образом. И здесь оптимисты предсказывают появление соответствующих бактериальных препаратов в ближайшем будущем.
Футурологи, пытаются предсказать будущее, приходят к печальному прогнозу. Если сельское хозяйство будет развиваться прежними путями, к 2000 г. на Земле будет недоедать около 2 млрд. людей. Требуются новые, оригинальные решения для того, чтобы обеспечить человечество пищевыми продуктами, и в первую очередь белком. Большую помощь в этом может оказать генная инженерия.
Сельское хозяйство к 2000 г. должно основываться на новых сортах растений, в первую очередь злаковых и бобовых. Пшеница, рожь, рис, кукуруза, соя и другие зернобобовые долго еще останутся основными кормильцами человечества. Но они приобретут невиданные свойства. Будущие злаки, как и бобовые, смогут обогащать почву азотом, не нуждаясь в азотных удобрениях, благодаря симбиотическим азотфиксирующим бактериям. Они освободятся от вирусов и приобретут устойчивость к грибковым и бактериальным заболеваниям. Наконец, зерно их будет содержать значительно большее, чем сейчас, количество белков, в первую очередь богатых незаменимыми аминокислотами. Хлеб из такого зерна по пищевой ценности приблизится к мясу или рыбе. Все это возможно было бы сделать уже сейчас или в ближайшие 10-15 лет.
Сейчас же каждую весну на миллионах гектаров поверхность планеты скальпируется плугами и боронами, насыщается инсектицидами и минеральными удобрениями. И все это ценой затрат огромного труда, расхода невосполнимых нефтепродуктов. И так с весны до осени, каждый год. В результате площадь, пригодная под пашню, сокращается, земля разъедается эрозией. Еще больший вред приносит засолонение поливных полей, занятых хлопком и рисом. Пустыня наступает везде, не только в Сахаре. Ф. Энгельс предсказывал это, когда писал, что за каждый крупный успех природа мстит человеку.
Где же выход? Его давно предсказывали ученые. Соратник Ч. Дарвина А. Уоллес писал, что со временем сахарная пальма вытеснит сахарный тростник, "так как для ее культуры не нужно ни удобрения, ни обработки земли, да и почва истощалась бы далеко не так быстро". Может быть, А. Уоллес ошибался относительно именно пальмы: похоже, углеводами нас обеспечит биотехнология. Но общий принцип угадан правильно - деревья вместо однолетних трав!
Наш известный палеонтолог, геолог и писатель- фантаст И. А. Ефремов так характеризует сельское хозяйство через тысячу лет: "...отпало трудоемкое ежегодное выращивание травянистых и кустарниковых растений. Деревья, долголетние, слабее истощающие почву, устойчивые к климатическим невзгодам, стали основными сельскохозяйственными растениями".
Итак, деревья - хлебные и ягодные, плодовые и ореховые, которые можно выращивать и на склонах гор, не истощающие и не иссушающие почву. Прообраз их - яблоневые и ореховые леса предгорий нашей средней Азии.
Если деревья выгоднее - почему земледельцы так привержены к однолетним злакам? Необходимо помнить, что революционная перестройка жизненно важной отрасли - дело неимоверно трудное.
Сто лет назад великий химик Д. И. Менделеев сказал: "Нефть не топливо, топить можно и ассигнациями". Сейчас слова его приобрели еще больший смысл. Ведь из нефти мы можем делать не только пластмассы, полимеры, красители, лекарства и многое другое, но и, применяя биотехнологические методы, кормовой и пищевой белок. А нефть до сих пор "вылетает в трубу", вернее в выхлопные трубы двигателей внутреннего сгорания.
Замены двигателю внутреннего сгорания на автомобилях, тракторах, комбайнах, стационарных дизелях до сих пор нет. Экономичные и легкие электрические аккумуляторы еще не вышли из стен лабораторий. И нескоро они вытеснят дизеля: надо закрывать тысячи старых заводов, строить тысячи новых, переучивать сотни тысяч специалистов.
Злаки пока еще заменить нечем. Хозяйственно ценные деревья (или хотя бы кустарники и многолетние злаки), которые пришли бы им на смену, еще придется создавать. И генная инженерия здесь должна сказать свое слово.
По-видимому, растениеводство - вторая после медицины отрасль практической биологии, в которой генноинженерные методы произведут решающие, революционные перестройки. Конечно, мы будем и дальше улучшать сорта пшеницы и других однолетников, потому что должны заботиться о себе и своих детях. Но мы должны подумать и о внуках и правнуках. А это значит, что вопрос о коренной перестройке растениеводства науке нужно решать уже сейчас. Ведь вопрос о выведении новых пород и видов деревьев с заданными свойствами настолько сложен, что для его разрешения и испытания в практике требуются многие десятилетия. И решать его придется кому-то из читателей нашей книги.
Минитракторы с гарантией от производителя. Подробности о покупке и гарантии на сайте.
|
ПОИСК:
|
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'