
Глава 7. Генная инженерия и практическая микробиология
Модное слово с неясным смыслом. Слово "биотехнология" в последнее время стало очень распространенным. Тем не менее мало кто из неспециалистов представляет, что обозначает это звучное название. Порой его трактуют чересчур широко: как отрасль народного хозяйства, где производятся любые манипуляции с живыми организмами и техникой одновременно. Что же такое биотехнология в строгом смысле этого слова?
Биотехнология - это химическая бионика. Как вы знаете, бионика - это использование секретов живой природы с целью создания более совершенных технических устройств. Одно время она была очень популярна. Однако далеко не все "патенты" живой природы можно перенести в металл и пластмассу, получив при этом экономический эффект. Но два таких "патента" до сих пор вызывают жгучую зависть инженеров.
Первый из них - организация систем управления в нервной системе высших животных. Известно, что быстродействие ЭВМ намного больше, чем у нервных клеток. В ЭВМ импульс передается практически со скоростью света, в нейронах он принципиально не может идти быстрее скорости звука в водной среде. А до создания по-настоящему думающих машин, сравнимых с мозгом, еще очень далеко.
Второй - химические процессы в живых организмах. Современный инженер-химик, синтезируя то или иное вещество, применяет чаще всего высокие температуры, высокие давления, агрессивные среды (кислоты, щелочи). Отсюда неизбежны большие затраты энергии, да и реакционное оборудование приходится делать из дорогих, но стойких материалов: стекла, нержавеющей стали, а то и платины.
Вот почему химики с завистью смотрят на биохимические процессы, идущие в живых организмах: с небывалой скоростью, строго направленно, без побочных продуктов, да еще и при комнатной температуре, нормальном атмосферном давлении и в нейтральной среде. Современный химик в принципе может синтезировать даже белок, но, увы, стоимость такого белка окажется в тысячи раз дороже природного.
Нельзя ли использовать биохимические процессы в промышленном производстве? Этим и занимается биотехнология. Основа ее - использование биологических катализаторов - белков-ферментов, в мягких условиях осуществляющих нужную человеку реакцию. Собственно и второе распространенное название ферментов - энзимы - пришло из биотехнологии. В прошлом веке Э. Бухнер, изучая процесс брожения, вызываемый дрожжевыми клетками, открыл, что сами клетки для гликолиза углеводов необязательны. Достаточно сока, выжатого из дрожжей. Активное начало этого сока и получило название - энзим ("в дрожжах").
Биотехнологи в подавляющем большинстве случаев используют для работ ферменты и иные биохимические системы микроорганизмов - бактерий и дрожжевых грибков. Микроорганизмы чрезвычайно быстро размножаются на искусственных средах, у них малые размеры и соответственно очень велико отношение поверхности к объему, а значит, весьма интенсивен обмен. Поэтому раньше биотехнология называлась промышленной микробиологией.
На микробиологических заводах микроорганизмы выращивают в огромных количествах. "Сердце" такого завода - ферментер - цилиндрический сосуд из нержавеющей стали, объем которого при некоторых производствах достигает нескольких десятков или даже сотен кубических метров. В ферментер подается стерильная питательная среда, в которую вносится культура микроорганизма (например, дрожжей). Содержимое ферментера интенсивно перемешивается: в него подается кислород, поддерживается температура, оптимальная для роста клеток. Специальные датчики позволяют автоматам следить за рН среды, содержанием в ней различных химических веществ, ее температурой и т. д. После окончания процесса ферментации клетки отделяют от культуральной жидкости с помощью сепараторов и используют их для выделения необходимых веществ.
С незапамятных времен человек использовал свойства микроорганизмов, еще не подозревая о их существовании. Наиболее важной для примитивной древней биотехнологии была реакция гликолиза - бескислородного расщепления углеводов на углекислый газ и этиловый спирт или молочную кислоту. Люди выпекали хлеб из дрожжевого теста, изготовляли вино, пиво, уксус, кумыс, кефир, простоквашу, сыр, творог, изготовляли силос, солили капусту, огурцы - везде работала реакция гликолиза. Иные реакции использовались значительно реже (при замачивании стеблей льна, дублении кож). Эмпирически люди получали наиболее ценные штаммы нужных бактерий и дрожжей, многие из них были технологическими секретами.
Борьба за "сладкую" жизнь. Продемонстрируем успехи биотехнологии на конкретном примере, хотя бы на получении сахара. Углеводы (сахара) несколько условно можно разделить на три категории. Первая из них - моносахариды, состоящие из одной молекулы. Три моносахарида особенно важны в питании человека: глюкоза (декстроза, или виноградный сахар), фруктоза (левулеза) и галактоза (молочный сахар). Эти углеводы имеют сладкий вкус. Сладкий вкус имеют и димеры моносахаридов - дисахариды. Это лактоза (продукт соединения глюкозы и галактозы), мальтоза (глюкоза плюс глюкоза) и наиболее нам известная сахароза, или тростниковый и свекловичный сахар (глюкоза плюс фруктоза).
Но моносахариды могут полимеризоваться и дальше, образуя длинные, иногда ветвящиеся цепи полисахаридов. Если эти цепи не очень длинны, они расщепляются ферментами нашей пищеварительной системы до моносахаридов и усваиваются организмом. Это крахмал (полимер глюкозы), животный крахмал - гликоген и инулин, запасное вещество корневищ сложноцветных растений (полимер фруктозы). Все они съедобные и питательные, но не сладкие. Более длинные, содержащие свыше тысячи остатков моносахаридов, к тому же сшитые иными остатками цепи, не усваиваются организмом. Пример такого полисахарида - целлюлоза, или клетчатка, слагающая клеточные стенки у растений. В чистом виде целлюлоза в природе встречается редко (волокна льна и хлопка), в древесине к ней добавляется лигнин (полимер ароматичных спиртов) и гемицеллюлозы - полимеры, содержащие другие углеводы, кроме глюкозы.
В умеренных широтах человечество всегда испытывало дефицит сладких моносахаридов и дисахаридов. Источниками их были только ягоды, фрукты и мед. Ввозимая с юга тростниковая сахароза стоила дорого, а свекловичная появилась лишь в XIX в. Моно- и дисахариды к тому же легко сбраживаются дрожжевыми грибками до этанола, в результате чего получаются опьяняющие напитки. Как превратить целлюлозу или хотя бы крахмал в глюкозу? Любопытно, что первых успехов в этом направлении первобытный человек добился, применяя биотехнологию! Можно проделать простой опыт. Пережевывайте кусочек черного хлеба как можно дольше, до получаса, и заметите, что он приобретает сладкий вкус. Это фермент амилаза, содержащаяся в слюне, расщепляет крахмал хлеба до мальтозы.
Первобытные люди долго жевали крахмальные клубни и корневища, жвачку сплевывали в сосуд и сбраживали ее - получался опьяняющий напиток.
Конечно, такой "биотехнологический" способ сейчас нельзя применять для получения сладких углеводов: он не только негигиеничен, но и нетехнологичен. В настоящее время в промышленности используется при изготовлении пива лишь амилаза, содержащаяся в проросших зернах ячменя (солоде). А как использовать огромные, до недавнего времени практически неисчерпаемые запасы целлюлозы, содержащиеся в древесине, которая не атакуется амилазой?
В 1819 г. во Франции впервые удалось расщепить на глюкозу чистую целлюлозу льна и бумаги, гидролизуя ее серной кислотой. Затем кислота нейтрализовалась мелом и оседала в виде гипса. Получался сладкий продукт - патока. Еще легче патоку было получить из крахмала. Однако сахарную проблему с помощью патоки решить не удалось. Сырье - чистая целлюлоза льна - было дороговатым, а гидролизат из древесины содержал, кроме глюкозы, еще и продукты гидролиза лигнина и годился лишь для получения гидролизного спирта и выращивания кормовых дрожжей. У нас из этого спирта делали синтетический каучук, а за рубежом в смеси с бензином заправляли автомобили. Сейчас, правда, нефть подешевела, но страны, не имеющие своих месторождений, такие, как Бразилия, успешно разрабатывают это направление. Так, в Бразилии около 1 млн. автомобилей имеют двигатели внутреннего сгорания, работающие на чистом спирте, а 10 млн. автомобилей заправляются бензином, содержащим 10% этилового спирта.
В странах, богатых нефтью, большую часть этилового спирта получают в настоящее время из этилена. Химическая реакция, которая лежит в основе получения синтетического спирта, хорошо известна:
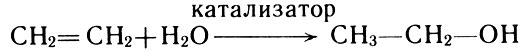
Этилен, в свою очередь, получают из нефти, запасы которой далеко не безграничны; поэтому биотехнологи всерьез думают об обратном процессе - получении этилена из этилового спирта, производимого микробиологическим путем. Ведь без этилена нельзя представить себе производство синтетических полимерных материалов и многих других ценных химических веществ.
Казалось бы, чистая технология (кислотный гидролиз) победила. Но победа была временной. Выясняя причину, почему во влажных тропиках быстро гниют хлопчатобумажные ткани, микробиологи нашли несколько видов микроскопических грибков, расщепляющих целлюлозу до растворимых, усваиваемых соединений. Грибки, поселяясь на ткани, выделяли ферменты, причем сразу несколько: одни из них расщепляли молекулы клетчатки на относительно длинные куски, другие - на димеры из двух остатков глюкозы, третьи - отщепляли по одному углеводному звену с конца молекулы. Сходные ферменты нашли у многих бактерий и актиномицетов, в том числе и у тех бактерий, которые живут в симбиозе с животными, потребляющими целлюлозу. Такие животные не столь уж редки: "белые муравьи" - термиты и ряд других насекомых, сверлящий дерево моллюск - "корабельный червь" могут питаться чистой клетчаткой, например фильтровальной бумагой. Некоторые из этих организмов - симбионтов могут усваивать атмосферный азот. Да жвачный рогатый скот: коровы, овцы, козы - могут усваивать клетчатку. Строго говоря, коровы питаются не клетчаткой травы, а продуктами ее переработки - симбионтами, обитающими в их сложных желудках.
Человек, видя такой заманчивый пример, также стал "приручать" микроорганизмы, расщепляющие клетчатку. И хотя сейчас кислотный гидролиз по-прежнему широко распространен, будущее за биотехнологическими методами.
Однако какое здесь место занимает генная инженерия? Раньше промышленные микробиологи выводили ценные штаммы простым отбором и подбирали комбинацию разных видов грибков. Теперь возникает возможность соединить все нужные для полного расщепления клетчатки ферменты в одной клетке. Когда такие штаммы пойдут в производство, можно будет постепенно сворачивать производство трудоемкой культуры - сахарной свеклы. Сахаром нас обеспечат дешевые отходы лесной промышленности. Дрожжевая масса к тому же - ценный источник кормового, а в будущем и пищевого белка. Но этого мало.
Хотя мировое человечество в среднем лишь на 70% обеспечено углеводами, в развитых странах, в том числе и у нас, наблюдается их явный избыток. Строго говоря, для нормальной жизни нам вполне бы хватало углеводов хлеба и картошки. С конфетами, шоколадом, вареньем, мороженым мы получаем огромный избыток Сахаров, который в условиях гиподинамии откладывается лишней массой (вернее сказать, лишним жиром) и пользы не приносит. Конечно, геологу в маршруте или альпинисту при восхождении глюкоза необходима, но мало кто сейчас сжигает лишние калории физической нагрузкой. Есть и люди, больные диабетом, для которых избыток углеводов, в первую очередь глюкозы, смертельно опасен.
Где же выход? Отказаться от сладкого вряд ли каждый сможет. Поэтому сейчас наблюдается стремление заменять тростниковый и виноградный сахар фруктовым - фруктозой. Она значительно слаще глюкозы, и потреблять ее можно в меньших количествах. Существует специальный фермент - глюкоизомераза, трансформирующий глюкозу в фруктозу. Он уже работает в промышленности.
При нехватке сахара его раньше заменяли суррогатом - сахарином. Он не так вреден, как представляют, но и пользы не приносит. Сейчас диетологи расхваливают заменители углеводов - сахарные спирты: сорбит и ксилит (первый получен из ягод рябины, второй - из дерева). Их получают, насыщая водородом соответствующие углеводы. Сорбит, например, дешевле всего получается гидрогенизацией глюкозы, а ксилит - из кукурузных кочерыжек.
Достоинства сорбита и ксилита помимо сладкого вкуса заключены в том, что они гораздо менее опасны для диабетиков, чем углеводы, широко применяются в промышленности при изготовлении самых разнообразных продуктов - от зубной пасты до взрывчатки. У ксилита есть еще одно ценное свойство: бактерии, вызывающие порчу зубов (кариес), его не усваивают; поэтому от конфет на ксилите зубы не болят.
Пока ученые не научились микробиологическим путем расщеплять лигнин древесины, пищевые продукты изготовляются из чистой целлюлозы и крахмала. Но есть микроорганизмы, потребляющие лигнин, и "приручение" их идет полным ходом.
В принципе возможны шоколад, конфеты и другие сладкие продукты, не содержащие ни глюкозы, ни фруктозы. Давно известны некоторые растения влажных тропических лесов - многолетние травы из семейства марантовых, приносящие очень сладкие плоды. Оказалось, что сладкий вкус этих плодов обеспечивают не углеводы, а белки. Известно несколько таких белков - монеллин и тауматины I и II. Тауматины в 10 000 раз слаще сахара и даже слаще сахарина, но в отличие от него безвредны. Казалось, что ничтожная добавка тауматина в пищу обеспечит "сладкую жизнь" без Сахаров. Генным инженерам удалось отклонировать ген тауматина, получить его экспрессию в бактериальных клетках и наработать этот белок в достаточных количествах. Однако выяснилось, что и тауматин далеко не идеальный заменитель сахара: он воздействует на другие вкусовые рецепторы и действие его очень длительное (после его применения во рту надолго остается сладкий вкус).
Гораздо более перспективным кажется использование аспартама - пептида, состоящего всего из двух аминокислот: аспарагиновой кислоты и фенилаланина. Добавленный в пищу в ничтожных количествах этот "сладкий пептид" полностью заменяет сахар. Разработаны как ферментативные, так и генноинженерные способы получения аспартама. Во всяком случае, биотехнологи планируют, что в 1990 г. производство этого вещества в развитых странах составит уже более 10 тыс. т.
Историю борьбы за сладкие углеводы завершим рассмотрением проблемы превращения глюкозы в целлюлозу, клетчатку с помощью биотехнологии.
Вы спросите: зачем нужно такое превращение? Ведь глюкозы не хватает, а целлюлоза в избытке? Правильно, однако в древесине целлюлоза загрязнена лигнином и гемицеллюлозами.
Чистая клетчатка, образующая длинные нитевидные молекулы, содержится только в волокнах льна и хлопка. Лучше же льняных и хлопчатобумажных тканей химики пока ничего не создали. Но лен и хлопчатник трудоемкие культуры, особенно хлопчатник. В Средней Азии и Закавказье он занимает лучшую землю, отнимает большую часть воды; уборка и очистка его весьма трудоемки. Хлопкоуборочные комбайны далеки от совершенства. Прежде чем их пустить на поля, нужно с хлопчатника удалить листья дефолиантами - небезвредными веществами. Может быть, выгоднее пойти по другому пути, отказаться от возделывания этих культур?
Есть такие бактерии - ацетобактерии, сбраживающие глюкозу до уксусной кислоты. Некоторые из них способны к реакции полимеризации глюкозы в клетчатку. Из клетки такой бактерии непрерывно вытягивается тройная нить целлюлозы - за час до 100 млн. глюкозных остатков! Для примера: средняя длина молекулы целлюлозы льна составляет 30 тыс. остатков, а хлопка - всего 1500; причем и хлопок, и лен растут весь летний сезон. Целлюлозные ленты, синтезируемые бактериями, образуют на поверхности культуральной среды пленку. В подсушенном виде это прекрасный перевязочный материал, по сравнению с которым обычные бинты не идут ни в какое сравнение. Возникла идея использовать бактериальную целлюлозу в текстильной промышленности.
К сожалению, глюкоза еще слишком дорога. Чтобы ткани, созданные бактериями, вошли в практику, нужно удешевить ее раз в 100. Впрочем, если учесть что ацетобактерий можно растить на дешевом гидролизате, учесть ту прибыль, которую можно получить от высвободившейся из-под хлопчатника земли и воды, экономию на очистке сырья, то эти планы покажутся не столь фантастическими.
Биотехнологи и генные инженеры пытаются гены, отвечающие за синтез целлюлозы, вставить в какие-нибудь фотосинтезирующие бактерии, которые сами вырабатывают глюкозу.
В отличие от большинства других микроорганизмов, требующих для роста сложных органических соединений, фотосинтетики используют для своей жизнедеятельности энергию солнечного света. Следовательно, для получения сверхвысококачественного текстильного сырья потребуется только солнечный свет, вода, воздух и минеральные соли. Быть может, кто-нибудь из вас решит эту задачу еще в нашем тысячелетии.
Представьте себе полностью автоматизированные заводы, стоящие где-нибудь в бесплодных пустынях, орошать которые невыгодно. Через огромные пластиковые реакторы, пронизанные солнечным светом, непрерывно прокачивается среда с бактериями. Сепараторы отделяют целлюлозу, которая направляется на прядильные фабрики. Побочным продуктом будет кормовая бактериальная масса. А на высвободившейся орошаемой земле цветут сады, растут овощи, фрукты, злаки - все то, что еще не под силу сделать биотехнологам.
А может быть, текстильщики будущего предпочтут материал лучше целлюлозных волокон? Вспомнили о прочных нитях паутины. Ведь пауки выпускают из своих желез тончайшую нить, по составу сходную с шелком тутового шелкопряда. Это тоже белок, богатый остатками аланина и глутаминовой кислоты, но прочность на разрыв доходит до 261 кг/мм2, т. е. в 6-8 раз крепче шелка! Паутинные ткани удивительно красивы, а в носке практически вечны. Но все идущие с древности попытки одомашнить пауков были неудачны. (Пауки на фермах просто пожирали друг друга, да и чем их кормить?) Теперь в Кембридже (Великобритания) генные инженеры пробуют вставить в геномы дрожжевых клеток выделенные ими гены белка паутины. Если это удастся, сверхценный текстильный материал будем получать из опилок, коры, щепок и прочих отходов деревообрабатывающей промышленности. Тогда главной продукцией лесозаводов будут паутинный шелк и кормовой белок, а доски и Древесностружечные плиты - побочным продуктом.
Эволюция биотехнологии. Так на частном, хотя и важном примере мы проследили три этапа развития биотехнологии. Начало первого - древней биотехнологии - уходит за тысячи лет назад, в древний каменный век. В этом периоде люди не подозревали о существовании микроорганизмов и ферментов, хотя и использовали их в своей хозяйственной деятельности.
Второй этап - этап промышленной микробиологии - начинается с середины XIX в, в первую очередь работами великого французского химика и микробиолога Луи Пастера. Люди уже знают о дрожжах и бактериях, культивируют и отбирают их полезные штаммы. Но биотехнологические методы по-прежнему применяются пока лишь в пищевой промышленности, реже в сельском хозяйстве (силосование, мочка льна).
Третий этап начинается в наше время. Биотехнология обретает свое теперешнее название. Этот период можно характеризовать следующими чертами:
1. Все чаще биотехнологи используют не сами клетки микроорганизмов, а выделенные из них ферменты. Это удобнее: нет побочных реакций, значительно облегчается стадия очистки конечного продукта.
Правда, сами по себе ферменты - вещества малоустойчивые; это белки с тонкой макромолекулярной структурой, легко разрушающейся под воздействием внешней среды. Речь, однако, идет об использовании их в качестве катализаторов промышленных процессов. Поэтому 10-15 лет назад в науке о ферментах возникло новое направление, получившее название инженерной энзимологии.
Одно из главных занятий инженеров-энзимологов - разработка методов закрепления ферментов на зернах твердого носителя. Таким носителем могут быть керамика, стекло, целлюлоза, а чаще всего синтетические полимеры. Закрепить, или, как говорят, иммобилизовать, белок на носителе можно разными способами: благодаря физической адсорбции, путем химического пришивания (образования ковалентной связи между функциональными группами белка и носителя) или посредством включения (захвата) его в полимерные гели, проницаемые для воды и низкомолекулярных веществ, но непроницаемые для белка.
Иммобилизованный фермент в десятки или даже сотни раз стабильнее фермента в растворе. Кроме того, его можно легко отделять от продуктов реакции или сам биохимический процесс вести непрерывно, прокачивая раствор реагентов, например, через колонку (проточный реактор), заполненную зернами носителя с закрепленным на них ферментом. Представьте себе реакционную колонку высотой метров в пять, заполненную иммобилизованной глюкозо-изомеразой. Сверху в колонку поступает раствор глюкозы (полученный, например, при гидролизе картофельного крахмала), а снизу вытекает ценный глюкозо-фруктозный сироп.
Еще пример. Как известно, дисахарид лактоза, или молочный сахар, для большинства людей полезен. Однако некоторые взрослые люди вообще не могут пить молоко только из-за того, что содержащаяся в нем лактоза не расщепляется из-за отсутствия 6-галактозидазы. В Африке этим недугом страдают целые племена. Безлактозное молоко можно легко получить с помощью иммобилизованного фермента - лактазы. Производство такого молока налажено, например, в Италии.
Развитие методов иммобилизации ферментов привело еще к одной важной находке. Оказалось, что часто вместо очищенного фермента выгоднее иммобилизовать на полимерном носителе целые клетки, производящие этот фермент. Для этого клетки микроорганизма заключают в полимерный, например полиакриламидный, гель (точно такой же, который используют для электрофореза нуклеиновых кислот), а затем кусочками этого заполняют проточные реакторы. Клетки способны многие десятки дней, а иногда и многие месяцы функционировать в таком состоянии (и даже размножаться внутри зерен геля). С помощью таких клеток - катализаторов - производят сейчас аминокислоты, антибиотики, стероидные гормоны, сахара. Их используют при очистке сточных вод, обезвреживая их от таких химических ядов, как бензол, фенолы, или даже от радиоактивных веществ.
Применяя иммобилизованные клетки, биотехнолог использует по сути дела все преимущества традиционной промышленной микробиологии и новой инженерной энзимологии. Именно здесь особенно большие надежды возлагаются на генетическую инженерию. Ведь промышленный процесс ведут не сами клетки, а фермент, который в них нарабатывается. Генная инженерия позволяет получить клетки с повышенной концентрацией необходимого фермента. Такие клетки называют сверхпродуцентами данного белка. Для этого достаточно увеличить в клетке число генов, кодирующих интересующий нас биокатализатор, например, ввести в них мультикопийную плазмиду с геном этого белка.
2. Вторая особенность современной биотехнологии - расширение ее сферы деятельности. Биотехнологическими методами сейчас изготовляются не только пищевые продукты, но и витамины, антибиотики, гормоны и ряд других лекарств, а также незаменимые аминокислоты. Производство последнего продукта имеет важное значение в животноводстве, особенно в производстве кормов для свиней и домашней птицы. Следует помнить, что организм животных не может сам синтезировать некоторые аминокислоты, он должен получать их с пищей. Человек, например, не может существовать, не потребляя триптофана, фенилаланина, лизина, треонина, валина, метионина, лейцина и изолейцина (ежедневно не менее 1 г каждого из них). Детям нужен еще и аргинин.
Растительные белки хлеба, картофеля, овощей и фруктов не сбалансированы по этим аминокислотам. Их там, как правило, меньше, чем в животных белках. Вот почему человек должен или потреблять большие количества того же хлеба, или добавлять в диету животный белок яиц, молока и мяса. Но свиней и кур кормить животным белком невыгодно. (У жвачных животных - рогатого скота - положение лучше: выше мы сказали, что корова, строго говоря, питается не сеном, а симбиотическими микроорганизмами, а у тех белок сбалансирован по аминокислотам.)
Выходов из этого положения два: добавлять в корм или животный белок (например, дрожжи), или незаменимые аминокислоты, недостающие в растительном корме. Второй путь выгоднее, поэтому биотехнологи работают над выведением бактерий - продуцентов лизина и триптофана. В этом случае потребление кормов резко снижается без ущерба для роста животных. Сейчас экономия растительного корма достигается чаще добавками дрожжевого белка, получаемого из гидролизата древесины и отходов сахарной и рыбной промышленности. Но производство незаменимых аминокислот перспективнее.
Рассмотрим вкратце, как генные инженеры конструируют штаммы бактерий со сверхпродукцией незаменимых аминокислот. Аминокислоты образуются в клетке вследствие очень сложного и многостадийного процесса, в котором участвуют многие ферменты. Этот процесс можно схематически изобразить в виде цепочки биохимических реакций
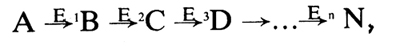
где буквами А, В, С, Д,..., N обозначены продукты реакций, a E1, Е2,... и т. д. - ферменты, катализирующие образование этих продуктов.
Известно, что образование любого вещества в клетке отрегулировано очень точно. В случае образования аминокислот эта регуляция в основном осуществляется по так называемому механизму обратной связи. Поясним, что это такое. Предположим, что N - аминокислота лизин. Если в клетке синтезировалось лизина больше, чем необходимо для ее нормальной жизнедеятельности, то избыток этой аминокислоты сам подавляет свой синтез. Воздействует, однако, не на фермент Еn, а на самый первый фермент в цепи реакций, т. е. на Е1, подавляет его активность и тем самым понижает уровень образования всех продуктов в цепи (В, С, Д) и т. д. Для клетки такой механизм очень экономичен: ведь если не нужен лизин, то не нужны и его предшественники.
Следовательно, чтобы сделать клетку сверхпродуцентом по лизину, необходимо растормозить реакцию А→В, сделав фермент Е1 нечувствительным для лизина. А это, как вы догадываетесь, поле деятельности для белковых инженеров. Зная, на какой участок E1 воздействуют лизины, они с помощью генной инженерии произведут соответствующие изменения в гене этого белка.
Таким и сходными путями идет сейчас получение сверхпродуцентов многих незаменимых аминокислот. В нашей стране эту задачу решает большой коллектив ученых Института генетики и селекции промышленных микроорганизмов под руководством В. Г. Дебабова. В микробиологической промышленности уже несколько лет "трудится" полученный ими сверхпродуцент лизина, производящий ежегодно более 40 тыс. т этого ценнейшего продукта.
В будущем биотехнология, очевидно, освоит производство не только кормового, но и пищевого белка из микроорганизмов, растущих на дешевых отходах. Уже сейчас из такого белка получают искусственное мясо и даже черную икру - вполне доброкачественные продукты. Трудность заключается в том, чтобы научиться искусственно получать те добавки, которые делают вкус этого мяса приемлемым (очищенный белок безвкусен). Добавим, что есть бактерии, хорошо растущие на нефти и природном газе - метане. Вопрос - в очистке бактериальной массы.
Приведем еще пример. Вы, наверное, знаете о стиральных порошках с ферментными добавками, которые расщепляют жиропот и прочие загрязнения. Получают их из бактериальной массы. Однако здесь есть противоречие: поверхностно-активные вещества - основа всякого стирального порошка - лучше всего работают при высокой температуре (80-90° С), а ферментные добавки в горячей воде теряют активность. Поэтому такими порошками следует стирать при 50°С, не выше. Есть, впрочем, бактерии-термофилы, хорошо себя чувствующие при температурах 90-100°С при атмосферном давлении и при 250°С - на больших глубинах океана, в подводных горячих источниках. Их ферменты: амилазы, протеазы и липазы - устойчивы и в горячей воде остаются активными. Можно было бы, конечно, выращивать на заводах термофилов, но они требуют совсем иной технологии. Фактически это означает отказаться от старых заводов и построить новые.
Английские генные инженеры нашли иной выход. Они встроили гены нужных, устойчивых к высокой температуре ферментов в геном обычной бактерии- продуцента Bacillus licheniformis, и стиральные порошки "заработали" при высокой температуре.
Биотехнология проникла даже в производство металлов. Корни биометаллургии также уходят в седую древность: первое железо было выплавлено человеком из болотных руд - продукта жизнедеятельности железобактерий, которые накапливают железо из воды, переводя его из двухвалентного в трехвалентное. Для бактерий это источник энергии, а побочный продукт - Fe2О3, оседающий на дно водоемов. Теперь биотехнология заняла прочное место в металлургической промышленности. Только в США 10% всей меди добывается микробиологическим способом; причем себестоимость ее в 2-3 раза ниже, чем стоимость меди, получаемой обычным путем. В металлургической промышленности ряда стран микроорганизмы используются для выщелачивания урана из руд, в процессе которого они из нерастворимого состояния переходят в растворимую форму. В СССР разработана технология бактериально-химического способа извлечения золота и серебра из бедных, этими металлами пород. Биометаллургия экономически выгодна; кроме того, она исключает загрязнение окружающей среды.
С каждым годом растет интерес к биотехнологии и со стороны нефтяников. Известно, что богатые нефтяные месторождения становятся все менее доступными. В то же время современные методы добычи позволяют извлечь из месторождения не более 40% содержащейся в нем нефти. Однако существуют микроорганизмы, разжижающие нефть или превращающие ее в газ. Есть надежда с их помощью оживить старые и уже заброшенные нефтяные месторождения в европейской части нашей страны. Имеются и первые результаты: в частности, одна из старых скважин в Башкирии (некогда богатейшее нефтью второе Баку) за полтора года с помощью микроорганизмов дала 160 тыс. т нефти. По последним данным, с помощью микроорганизмов удается каменный уголь превратить в жидкое топливо, схожее с нефтью.
3. И наконец, третья особенность современной биотехнологии - в нее широко внедряется генная инженерия. Нужные штаммы микроорганизмов теперь получаются не только отбором случайно возникающих мутаций, но и вставкой плазмид с соответствующими генами. Именно генная инженерия необычайно расширила возможности биотехнологии, позволив получать бактерии со свойствами, прежде небывалыми.
Завершим главу совсем новым примером. Генным инженерам удалось перенести в клетки кишечной палочки, продуцирующие большие количества аминокислоты триптофана, ген из другой бактерии, в котором закодирован фермент, окисляющий производные бензола. В кишечной палочке этот фермент окисляет триптофан так, что в конечном итоге образуется краситель индиго. Индиго известно людям с незапамятных времен. До конца прошлого века его вывозили из индийских колоний Англии, где краситель добывали из индигоносных растений. Потом химики придумали способ получения индиго из анилина, и синтетический краситель вытеснил природный. И вот теперь не исключено, что природный индиго (хотя и созданный при прямом участии человека) вновь вытеснит синтетический.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'