
2.4. Методы обработки данных
Ряд разделов клинической иммуногенетики не может полноценно развиваться без соответствующего математического аппарата. Помимо общепринятых методов статистической обработки результатов, для целей клинической иммуногенетики были созданы специальные расчеты и формулы, позволяющие оценивать флюктуирующий клинический материал и используемые в таких (основных) клинико-практических направлениях, как популяционное иммуногенетическое обследование, оценка эффективности аллогенных пересадок, ассоциативные связи HLA с болезнями.
2.4.1. Расчет частоты антигена, частоты гена и гаплотипа в популяционных обследованиях
В плане наследования антигенов гистосовместимости человеческая популяция является панмиктической и подчиняется закону Харди - Вейнберга, выражающемуся формулой наследования для системы с двумя признаками:
p2 + 2pq + q2 = 1,
которая отражает количество гомо- и гетерозиготных по соответствующему гену индивидов в выборке.
Частота антигена рассчитывается как процентное (долевое) соотношение индивидуумов, несущих антиген к общему числу обследованных, а частота гена - по указанной выше формуле после ее преобразования:
p2х + 2рх(1 - pх) + (1 - рх)2 = 1;
Но так как
р2x + 2рх(1 - рх) = Ах,
то
1 - px = √1 - Ax и px = 1 - √1 - Ax
где рх - частота гена, а Ах - антигена.
Определенная по формуле частота гена должна быть проверена путем сравнения наблюдаемого в выборке распределения гомо- и гетерозиготных индивидуумов с теоретически рассчитанным в соответствии с формулой равновесия Харди - Вейнберга. Формулы, по которым производится теоретический расчет, и схема манипуляций в соответствующей выборке приведены в табл. 25.
Таблица 25
Схема проверки частоты гена
| Обозначение фенотипа | Генотип | Теоретически ожидаемое число индивидуумов |
| P | PP, BB | N·(P2 + 2PB) |
| Q | QQ, QB | N·(Q2 + 2QB) |
| PQ | PQ | N·2PQ |
| B (blank) | BB | N·B2 |
Обозначения: N - число индивидуумов в выборке; В - пустой аллель.
Важным элементом популяционного анализа является гаметная ассоциация, которая учитывает разницу в теоретически определенной ассоциации между двумя антигенами разных локусов и истинной ассоциацией, встречаемой в популяции. К необходимости введения данного показателя приводит следующее рассуждение: если бы аллели локусов А и В встречались независимо друг от друга, частота их ассоциации на хромосоме (гаплотип) определялась бы произведением Р1xР2, где Р1 и Р2 - частоты соответствующих генов. Однако в популяции сочетания отдельных аллелей встречаются более часто или, наоборот, более редко, чем это следует из теоретического расчета, т. е. данные гены находятся в состоянии неравновесного сцепления (linkage disequilibrium), которое измеряется величиной Δ, отражающей превышение или дефицит гаплотипа в популяции по сравнению с произведением частот двух генов.
Величина Δ подсчитывается из "сетки" 2x2" (см. 3.1) по формуле P. Mattius (1970):
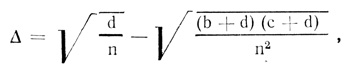
где n - число обследованных в выборке; b - число индивидов, несущих А и не имеющих В; с - число индивидов, несущих В и не имеющих A; d -число индивидов, не несущих ни А, ни В.
Приведенная формула входит составной частью в формулу, используемую для определения частоты гаплотипа в панмиктической популяции:
РАВ = (РАВ × РB) + ΔАЗ,
где РА и РB - частоты соответствующих генов; а ΔАB - гаметная ассоциация между генами А и В.
2.4.2. Оценка эффективности клинических аллотрансплантаций (актуриальная выживаемость)
Оценка результативности трансплантации любого органа представляет определенные трудности, поскольку "кривая выживаемости" трансплантатов не может быть выражением простого процента от исходного уровня, принимаемого за 100. Для определения выживаемости трансплантатов в конкретный срок (1 или 2 г) исследователь не в силах произвести в начальной точке отсчета статистически значимое количество операций с тем, чтобы подсчитать процент гибели к концу интересующего периода, так как пересадки производятся не одномоментно.
Для оценки эффективности трансплантаций был создан метод актуальной выживаемости, принятый во всех крупных трансплантологических объединениях [Busson М., Hors J., 1976], который позволяет определить эволюцию кривой выживаемости, не дожидаясь конечной судьбы каждого трансплантата.
Метод основан на следующих принципах:
1. Эволюция всех трансплантатов соотносится к единой нулевой точке отсчета и производится оценка гибели и выживаемости по периодам (3, 6, 9, 12 мес и т. д.).
2. Каждая "остановка" трансплантата рассматривается только один раз, в тот период, когда она произошла, и не учитывается в дальнейшем.
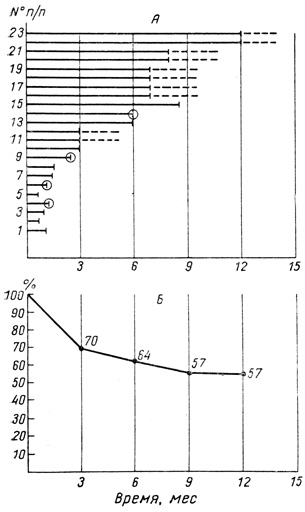
Рис. 17. Сроки жизни трансплантатов по периодам (для вычисления актуариальной выживаемости). А - кружком отмечены больные, умершие при функционирующем трансплантате; вертикальной черточкой - 'остановка', т. е. больные, у которых трансплантат не функционирует или которым произведено хирургическое изъятие; пунктир означает, что к концу рассматриваемого периода трансплантат существует уже определенное время (3, 6, 9 мес) и продолжает функционировать; Б - по оси абсцисс - периоды жизни трансплантатов: в период 3 мес 'вступают' 23 трансплантата и 'останавливаются' № 1, 2, 3, 5, 7, 8, 10; в период 6 мес 'вступают' № 11 - 23 и 'останавливается' № 13; в период 9 мес 'вступают' № 15 - 23 и 'останавливаются' № 15, а в период 12 мес 'вступают' № 22 и 23, 'остановившихся' нет
Рассмотрим пример построения кривой актуариальной выживаемости. На рис. 17, А представлены конкретные сроки жизни группы трансплантатов, соотнесенные к единой нулевой точке отсчета. Для каждого отрезка времени (3,6 мес и т. д.) вычисляется несколько показателей: фракция гибели (Q), равная отношению числа трансплантатов, прекративших функционировать в течение данного периода, к числу трансплантатов, действующих в начале этого периода; фракция выживаемости (S), равная разности I - Q; процент выживаемости (Tn), который определяется умножением фракции выживаемости данного периода (п) на процент выживаемости предыдущего периода (n - 1), т. е. Tn = SnхTn-1.
В табл. 26 приведены конкретные цифровые значения для каждого из периодов согласно данным рис. 17, А.
Таблица 26
Пример вычисления актуариальной выживаемости по периодам
| Исходные данные и параметры отсчета | Время, мес | |||
| 3 | 6 | 9 | 12 | |
| Действующие трансплантаты (Д) | 23 | 13 | 9 | 2 |
| Остановившиеся (О) | 7 | 1 | 1 | 0 |
| Q = О/Д | 0,30 | 0,80 | 0,11 | 0 |
| S = 1 - Q | 0,70 | 0,92 | 0,89 | 1 |
| Tn = Sn×Tn-1 | 0,70 | 0,64 | 0,57 | 0,57 |
| ES | ±0,18 | ±0,20 | ±0,16 | ±0,13 |
Построение кривой выживаемости за 3 мес: к началу этого периода действуют 23 трансплантата (Д); в течение периода перестают функционировать 7 (О); следовательно, Q = 7/23 = 0,30; S = 1 - 0,30 = 0,70, а Т3 мес = 0,70 × 1 = 0,70 (70%).
Построение кривой выживаемости за период от 3 до 6 мес: в начале этого периода в соответствии с рис. 17 продолжает действовать 13 трансплантатов; перестает функционировать 1; тогда Q = 0,08; S = 0,92; Т6 мес = 0,92 × 0,70 = 0,64 (64%) и т. д.
На рис. 17, Б изображена кривая актуариальной выживаемости, построенная на основе данных рис. 17, А.
В том случае, когда сравнивается выживаемость двух групп трансплантатов, необходимо рассчитывать доверительный интервал для каждой точки кривой по следующей формуле:
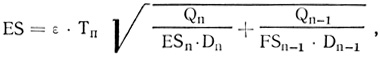
где ε = коэффициент, равный 1,96 при р = 5%, а Dn, Dn-1 - число трансплантатов в начале каждого периода. Для точки 6 мес в нашем примере:
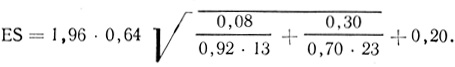
Трансплантаты, срок жизни которых к концу рассматриваемого интервала времени составил ровно 3,6 мес и более, но которые продолжают успешно функционировать, должны засчитываться в рубрике Д для следующего периода (n + 1), но не должны учитываться в периоде n + 2, поскольку теоретически они могут погибнуть в периоде n + 1. Так, например, трансплантат № 11 в конечной точке учета просуществовал ровно 3 мес и продолжает функционировать далее; он учитывается как действующий для периода 6 мес, но уже не учитывается для периода 9 мес.
2.4.3. Вычисление ассоциативных связей между HLA и болезнями
При оценке данных взаимоотношений необходимо ответить на два вопроса:
- существует ли разность между частотой носителей антигена в группе пациентов и в группе здоровых лиц и имеет ли она статистическую значимость?
- как сильна ассоциация между антигеном и болезнью?
Для ответа на первый вопрос используют критерий χ2, прибегая к построению "сетки 2 × 2" (см. 3.1), где а - больные носители антигена; b -здоровые носители антигена; с - больные, не несущие антигена, и d -здоровые, не несущие антигена:
χ2 = N(ad - bc)2/(a + b) (a +c) (b + d) (c + d); N = a + b + c + d.
Пример: в выборке из 44 больных антиген В13 присутствует у 12 человек; в контрольной группе здоровых людей тот же антиген присутствует у трех из 89 человек. Тогда
χ2 = 133[(12 × 86) - (3 × 32)]2/15 × 44 × 89 × 118 = 16,66.
Определение достоверности различий и достоверности наблюдаемой: ассоциации производится по таблицам χ2 при учете одной степени свободы.
В клинической практике широко употребим другой метод, отвечающий на вопрос о силе ассоциации между антигеном и болезнью и называемый критерием относительного риска [Woolf В., 19551.
Биологический смысл показателя - риск развития заболевания у носителей антигена по сравнению с индивидами, не несущими данный антиген:
R = fп (1 - fк)/fк (1 - fп),
где fп - фракция носителей антигена среди пациентов; fк - фракция носителей антигена в контрольной группе.
Используя данные приведенного выше клинического примера, получаем:
R = 0,273 (1 - 0,034)/0,034 (1 - 0,273) = 10,676.
В данном случае fп и fк выражаются в десятичных дробях или процентах.
Показатели относительного риска более двух считаются значимыми.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'