
5.3.1* Расшифровка структуры нативных гяРНП
Литература: [211, 212]
Весной 1967 г. я обратил внимание на статью Г. Лоуфорда и соавт. (Канада), в которой сообщалось о выделении полисом из клеточных ядер с помощью экстракции в присутствии ингибитора РНКазы из цитоплазмы печени крысы. Анализ рисунков статьи вызвал у меня подозрение, что полученные автором "полисомы" вряд ли являются на самом деле полисомами, а, возможно, соответствуют искомым нами частицам. Наиболее же важным для нас было сообщение об использовании ингибитора РНКазы. О. П. Самарина и ее аспирант Е. М. Луканидин в несколько дней получили цитоплазматический ингибитор нуклеазы и провели выделение ядерных частиц обычным нашим методом, но с добавкой ингибитора ко всем экстрагирующим растворам. Результаты превзошли все ожидания. В сахарозном градиенте вместо одного пика 30S-частиц появилась серия дискретных пиков с коэффициентами седиментации 30S, 47S, 56S, 60S и т. д., вплоть до 100-200 S, которые содержали новообразованную РНК (рис. 36). Эта РНК по нуклеотидному составу соответствовала ДНК. Наиболее существенным явилось наблюдение, что если обработать тяжелые частицы строго подобранной дозой РНКазы, то меченая РНК количественно переходит в 30S-частицы. Следовательно, тяжелые РНП состоят из серии мономеров, SOS-частиц, соединенных цепью РНК точно в соответствии с исходным предположением.
![Рис. 36. Выделение нативных ядерных РНП-частиц. а - ультрацентрифугирование в сахарозном градиенте ядерного экстракта из клеток печени крысы, полученного в присутствии ингибитора РНКазы (А). На седиментограмме - серия дискретных пиков, от 30S до 150S. После мягкой обработки РНКазой (Б) почти вся меченая РНК(клетки метили в течение 30 мин |14С]-оротовой кислотой) перемещается в ЗОБ-пик; б - ультрацентрифугирование частиц из разных областей сахарозного градиента в градиенте плотности Cs-CI (после фиксации формальдегидом; А - 30S-частицы, Б - 60S-частицы, В - 100S-частицы.](pic/000047.jpg)
Рис. 36. Выделение нативных ядерных РНП-частиц. а - ультрацентрифугирование в сахарозном градиенте ядерного экстракта из клеток печени крысы, полученного в присутствии ингибитора РНКазы (А). На седиментограмме - серия дискретных пиков, от 30S до 150S. После мягкой обработки РНКазой (Б) почти вся меченая РНК(клетки метили в течение 30 мин |14С]-оротовой кислотой) перемещается в ЗОБ-пик; б - ультрацентрифугирование частиц из разных областей сахарозного градиента в градиенте плотности Cs-CI (после фиксации формальдегидом; А - 30S-частицы, Б - 60S-частицы, В - 100S-частицы.
Более детальный анализ показал структурную однородность тяжелых частиц. Ультрацентрифугирование фиксированного материала в градиенте плотности хлористого цезия показало, что частицы любого размера имеют одну и ту же плавучую плотность (1,41 г/см3), т. е. отношение РНК/белок в них одинаково. При электронной микроскопии в ЗОБ-пике были видны отдельные компактные частицы, в 475-пике - димеры, в 70-75S-30He - тетра-и пентамеры и в 90-100S-зоне - октамеры. Таким образом, дискретность пиков обусловлена тем, что в каждом содержится целое число 30S-частиц. Размеры РНК возрастают пропорционально размерам частиц. В 308-части-цах присутствовала 8.5S - PHK, в димерах - 14S, тримерах - 16,8S, пентамерах - 21S-PHK и в 120- ШБ-частицах - гетерогенная РНК с пиком в области 32S. Расчеты показывают, что на мономер в каждом случае приходился отрезок РНК длиной около 600 нуклеотидов.
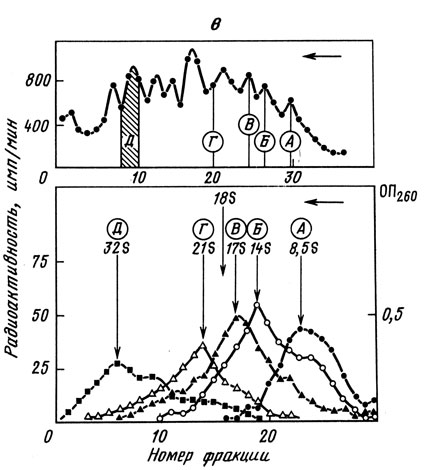
Рис. 36. Выделение нативных ядерных РНП-частиц. в - размеры РНК из разных фракций ядерных РНП-частиц. Наверху - седиментограмма ядерных РНП, полученных в присутствии ингибитора РНКазы. Из отдельных пиков (указанных буквами) выделяли РНК и рецентрифугировали ее в сахарозном градиенте (более длительное время). Цифры указывают коэффициенты седиментации этих РНК (для максимумов). 28S и 18S - маркеры рРНК
Наконец, был изучен белковый состав частиц. Эти опыты вначале велись работавшим в нашей лаборатории научным сотрудником из Венгрии Я. Молнером. В первых экспериментах была использована система электрофореза в полиакриламидном геле в ацетатном буфере рН 4,5, содержащем мочевину. При этом происходило разделение белков и по заряду, и по молекулярной массе, но одновременно могла происходить и потеря некоторых белков. В 30S-частицах были выявлены три главные полосы. Совершенно аналогичные полосы выявлялись и в более тяжелых частицах. Таким образом, и по белковому составу поличастицы и моночастицы совпадали.
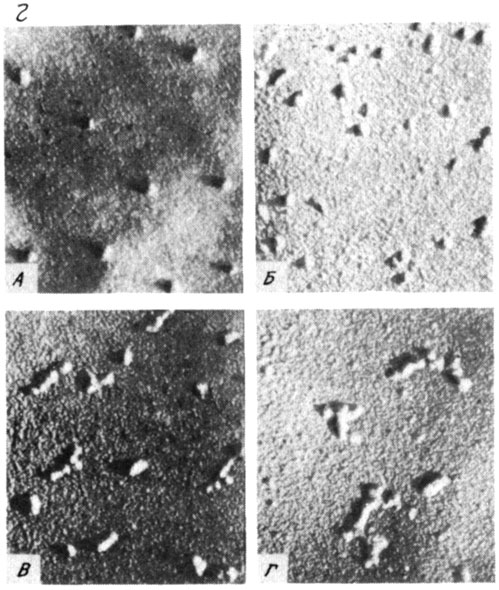
Рис. 36. Выделение нативных ядерных РНП-частиц. г - электронная микроскопия ядерных РНП из разных зон сахарозного градиента (метод напыления); А - 30S-частицы, Б - 45S-зона (димеры), В - 70-75S-зона (гетра- и пентамеры), Г - 90-100S-зона (по результатам, полученным О. П. Самариной, Е. М. Луканидиным и др.)
Учитывая полученные результаты, а также наши ранние данные, свидетельствовавшие о локализации РНК на поверхности частиц, мы предложили модель организации ядерных гяРНП, согласно которой высокомолекулярная РНК в ядрах наматывается на глобулярные белковые частицы, названные информоферами, т. е. носителями информационной РНК. На каждый информофер навивается отрезок РНК длиной ~600 нуклеотидов. Комплекс информофера и такой РНК образует мономер или 30S-частицу. Для обозначения 30S-частиц недавно предложен термин рибонуклеосома. Отдельные 30S-частицы соединены между собою короткими мостиками РНК, разрывы которых при РНКазной обработке ведут к переходу поличастиц в 30S-частицы. Эта модель прямо вытекает из данных, приведенных выше, и доказывается ими. Единственным недостаточно доказанным положением являлось положение о наматывании РНК на поверхность информофера, ибо оно базировалось в основном на результатах РНКазного переваривания. Поэтому в последующей работе мы обратили особое внимание на проверку именно этого предположения.
Следует отметить, что описанная для ядерных РНП частиц структурная организация явилась совершенно новым типом организации нуклеопротеида, когда нуклеиновая кислота наматывается на серию компактных белковых глобул, образуя цепочку бусин на нити. Позднее точно такой же принцип организации был описан, как известно, для хроматиновых фибрилл, нуклеосом (см. гл. 3), т. е. он является общим для главных полимеров клеточного ядра, ДНП и РНП. Однако лишь после открытия этого типа организации для нуклеосом он получил общее признание.
Вообще наши работы по РНП-частицам долгое время не находили широкого отклика. Часть западных авторов считали РНП-частицы артефактом. Другие опубликовали статьи, в которых пытались опровергнуть наши данные. Обычно опровержения базировались на неточном воспроизведении эксперимента на его решающих этапах. Лишь к середине 70-х годов наши работы стали получать многочисленные подтверждения, и в настоящее время описанная здесь структура РНП-частиц является общепризнанной.
Следующим этапом наших исследований (конец 60-х - начало 70-х годов) явилось уточнение структуры мономера, 30S-частиц, а также изучение их белкового состава.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'