
06.07.2019
Что такое эпитранскриптомика?
Для механизма, регулирующего работу генов — модификаций молекул РНК появился новый термин — эпитранскриптомика. Во второй половине июня в Чикагском университете прошла международная конференция по эпитранскриптомике. Кратко о ней рассказала редакция сайта журнала Science.
Ставшая классической схема работы генетических механизмов состоит из трех звеньев: ДНК > РНК > белки. Информация считывается с гена, расположенного в цепочке ДНК, при этом по принципу комплементарности синтезируется молекула информационной (или матричной) РНК. Далее матричная РНК попадает в рибосому, где служит схемой, по которой строится соответствующий данному гену белок. Синтез молекулы РНК по образцу ДНК называют транскрипцией, синтез белка по образцу РНК — трансляцией. Гены, записанные в ДНК, в таком случае оказываются неизменным стандартом и могут измениться только в результате мутации: при замене нуклеотида в цепочке ДНК, потере или вставке участка цепочки.
Схема эта, безусловно, верная, но в ней не учтён ещё ряд действующих факторов. И геном организма на самом деле работает не как шаблон для штамповки неизменных деталей и не как литейная форма, в которой одна за другой отливаются идентичные изделия. Скорее, геном можно сравнить с литературным сценарием, по которому разные режиссёры снимут похожие, но всё-таки отличающиеся фильмы. Или с оркестровой партитурой, которая под руководством разных дирижёров будет звучать по-разному. Дело в том, что в живой клетке существует целый ряд механизмов, которые влияют на работу генома. Они могут включать определённый ген, активируя его транскрипцию, или же выключать, подавляя эту транскрипцию. Работа клетки по синтезу белков при этом изменяется, хотя сама последовательность нуклеотидов в ДНК остаётся прежней. Все способы, которыми регулируется работа генов без изменения ДНК, называют эпигенетическими механизмами.
Таких механизмов существует несколько, и один из самых важных среди них — метилирование ДНК. Метильная группа (CH3) присоединяется к цитозину — одному из азотистых оснований в составе ДНК. Если в каком-то гене будет много таких метилированных участков, то фермент ДНК-полимераза, который занят считыванием информации с гена, обработать его не сможет. Соответственно, не будет построена соответствующая цепочка РНК (не произойдёт трансляция) и в конечном итоге не синтезируется белок, за который отвечает этот ген. Метилирование участков ДНК служит, таким образом, методом выключения определённых генов. Для правильной работы многих систем организма необходимо, чтобы определённые участки хромосом имели нужный «профиль метилирования», то есть чтобы метильные группы были присоединены в правильных местах. Известны даже болезни, связанные с нарушением профилей метилирования тех или генов.
Позже учёные обратили внимание на метилирование уже не ДНК, а информационной РНК. Впервые метилирование РНК было замечено ещё в 1970-х, но тогда ему не уделили внимания, так как в основном работали над изучением ДНК. Сейчас, благодаря методам, разработанным в последнее десятилетие под руководством Чуаня Хэ (Chuan He) из Чикагского университета, Сэмми Джеффри (Samie Jaffrey) из Корнелльского университета и Гидеона Рехави (Gideon Rechavi) из Тель-Авивского университета, стало возможным обнаружить метильные группы у молекул РНК. Обнаружилось, что метилированию подвержены самые разные молекулы РНК: транспортные, рибосомальные, информационные, малые, длинные некодирующие и микроРНК.
Метилирование ДНК и метилирование РНК отличаются тем, что у ДНК метилируется, как уже говорилось, цитозин, а у РНК метильная группа в 80 % случаев присоединяется не к цитозину, а к аденозину. Но, как и при метилировании ДНК, оно препятствует считыванию информации и блокирует активность гена, только не на этапе транскрипции, а на этапе трансляции. Отсюда и название эпитранскриптомика.
В 2012 году Гидеон Рехави и его коллеги описали одну из разновидностей метилирования РНК, которая обозначается m6A, где цифра обозначает номер позиции в молекуле аденозина, к которой присоединяется метильная группа. Осуществляет это особый фермент m6A-метилтрансфераза. Сейчас данный вид метилирования РНК обнаружен у самых разных организмов: млекопитающих, насекомых, растений, грибов, бактерий, есть он даже у вирусов. При этом у дрожжей и у бактерий m6A-метилированные нуклеотиды обнаружились с аналогичных участках рибосомальной РНК.
В Чикаго Чуань Хэ и его коллеги открыли, что существует и белок, производящий обратное действие, то есть удаляющий m6A-метки с молекулы РНК. Им оказался белок FTO, кодируемый геном, расположенным в шестнадцатой хромосоме.
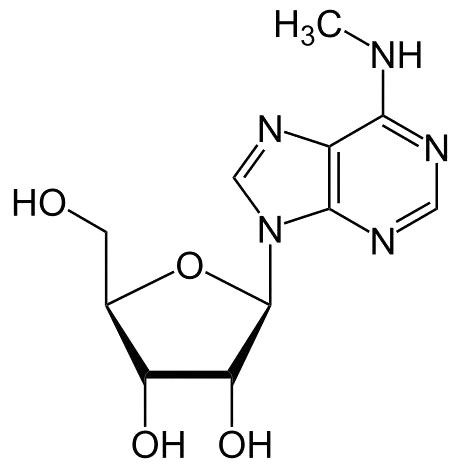
Формула N6-метиладенозина
В 2016 году в журнале Nature вышла совместная статья исследователей из США и Израиля, посвящённая ещё одному из типов метилирования РНК. На этот раз метильная группа присоединяется к аденозину в позиции номер 1 (m1A). В целом же учёные пришли к выводу, что количество метилированных нуклеотидов в РНК примерно в десять раз больше, чем в ДНК. Следовательно, роль метилирования РНК может быть очень важной.
Сейчас изучено несколько модификаций работы конкретных генов, осуществляемых при помощи метилирования РНК. Например, оно повышает экспрессию генов, необходимых для правильной дифференциации эмбриональных стволовых клеток в клетки разных типов. Иногда метилирование РНК оказывается вредным. Существует тип метилирования РНК, связанный с повышенным риском диабета. При миелобластном лейкозе добавление метильной группы в РНК клеток крови препятствует превращению стволовых клеток крови (миелобластов) в различные типы лейкоцитов. В 2017 году три группы учёных независимо показали, что удаление фермента, который добавляет метильную группу в информационную РНК, убивает опухолевые клетки при остром миелобластном лейкозе. Уже разрабатываются экспериментальные препараты для лечения лейкоза, основанные на данном эффекте. На нынешней конференции Тони Кузаридес (Tony Kouzarides) из Института имени Джона Гердона в Кембридже рассказал ещё об одном случае модификации РНК, связанном с возникновением лейкоза. Он поделился своими подозрениями, что таких явлений будет обнаружено ещё больше.
В новых экспериментах группы Чуаня Хэ было показано, что m6A-метилирование критически важно для развития мозга. Через белки, считывающие информацию с РНК, оно связано с контролем точного времени образования новых нейронов в мозге эмбрионов мышей, а также воздействует на восстановление аксонов после повреждения нерва. В одном из экспериментов Хэ и его сотрудники обнаружили, что m6A-метилирование связано ещё и с механизмами памяти. При отключении гена, который отвечает за белок, считывающий m6A-метки с РНК, у мышей возникали дефекты памяти, но после введения им вируса, несущего функциональный вариант гена, эти дефекты исчезали. Когда исследователи химически стимулировали нейроны, чтобы имитировать запоминание новой информации, они наблюдали резкий всплеск синтеза белка, связанного с m6A.
Выясняется, что модификация информационной РНК не ограничивается метилированием. В исследовании Шалини Обердёрфер (Shalini Oberdoerffer) было обнаружено, что помимо метилирования существует ацетилирование РНК, при котором группа CH3CO-присоединяется к цитозину. Такая модификация стабилизирует молекулу информационной РНК и, возможно, помогает ей соединяться с молекулами транспортных РНК.
Источники:
|
ПОИСК:
|
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'