
Глава 3. Как гены передаются из клетки в клетку
В 40-х годах нашего столетия полагали, что у микроорганизмов - прокариот, не имеющих оформленного ядра, нет полового процесса, нет и обмена генами. Однако опыты Ф. Гриффитса и Л. А. Зильбера свидетельствовали, что обмен генами у прокариот все-таки должен существовать.
Невидимые хромосомы бактерий. Сейчас известно по меньшей мере три формы обмена генами - рекомбинации у бактерий. Первый из них назвали трансформацией (превращением). Именно его обнаружил Ф. Гриффите. Трансформация происходит, когда ДНК из разрушенных клеток одной бактерии попадает в способные делиться клетки другой.
Названный процесс в природе встречается не так уж часто. Прежде всего далеко не все клетки в культуре бактерий способны к трансформации. Клетки, способные поглощать чужую ДНК, называют компетентными. Чтобы повысить процент компетентных клеток, нужно сохранить в целости молекулы фермента, на какое-то время открывающего оболочку бактерии для чужеродных генов. Для этого разработаны особые методы. Кроме того, чужая ДНК должна обладать определенным сродством к хозяйской ДНК; иначе включения в бактериальную хромосому не произойдет.
Впрочем, есть ли у безъядерных организмов хромосомы? Оказывается, есть. И о строении их узнали до того, как увидели в электронном микроскопе. Началось с того, что в 1946 г. американские генетики Дж. Ледерберг и Е. Тэтум открыли у бактерий процесс, удивительно похожий на половой процесс у ядерных одноклеточных - инфузорий, у которых он называется конъюгацией (соединением). Так, инфузории-туфельки соединяются попарно мостиками из цитоплазмы. Через эти мостики происходит обмен ядрами, а затем клетки расходятся. Следует отметить, что в этом случае привычное понятие "половое размножение" неточно. Это только у организмов, образующих гаплоидные гаметы, половой процесс (обмен генами) объединен с размножением. У инфузорий он отделен от размножения, обмен генами (рекомбинация) существует в чистом виде. Ведь после конъюгации остаются те же две инфузории, которые начали ее, но это рекомбинанты, обменявшиеся ядерным материалом.
Конъюгация у бактерий похожа на половой процесс инфузорий, пожалуй, только внешне. Прежде всего обмена генами здесь не происходит, передача ДНК односторонняя. Те клетки, которые отдают ДНК, называют донорами - "мужскими клетками". "Женские", акцепторные, клетки могут ДНК только принимать (рис. 20). Нить ДНК медленно, около полутора часов, перетекает из одной бактерии в другую по соединяющей их трубочке. Этот процесс можно в любой момент прервать, сильно встряхивая взвесь бактерий. Тогда соединяющая трубочка разорвется и в акцепторную клетку перейдет лишь фрагмент ДНК. Зная, с какой части бактериальной хромосомы начинается перенос, можно определить порядок расположения в ней генов.
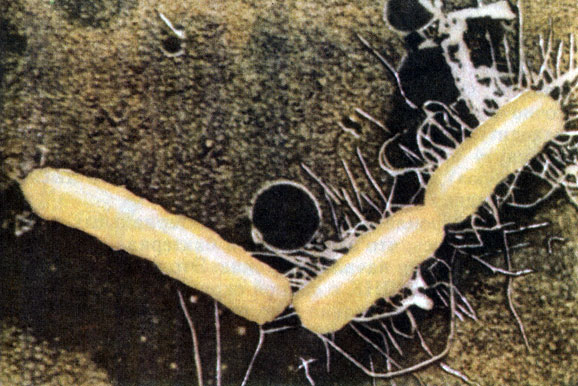
Рис. 20. Клетки кишечной палочки в момент конъюгации. Хорошо видны трубочки, по которым ДНК перетекает из клетки в клетку (с электронной микрофотографии)
По каким признакам генетики опознавали бактериальные гены? Чаще всего по способности бактерий синтезировать разные химические вещества, например аминокислоты. Обычный объект таких опытов бактерия кишечная палочка - Echerichia coli. Она может расти и в природных средах, но больше всего ее в кишечнике человека и в его экскрементах. Она постоянный спутник человека и свидетель загрязнения воды, почвы и пищевых продуктов.
Микробиологи, изучавшие бактерий недавно найденного в Магаданской области замороженного мамонтенка Димы, были очень огорчены: во всех посевах проросла вездесущая кишечная палочка. Удивляться нечему: перед появлением микробиологов мамонтенка смотреть сбежался весь поселок и не у всех руки были чистые.
Обычные, "дикие", штаммы кишечной палочки неприхотливы. Для них пригодна среда с глюкозой (источник углерода и энергии), фосфатом (источник фосфора) и какой-либо солью аммония (источник азота). Все аминокислоты и нуклеотиды они синтезируют сами. Это организмы-прототрофы. Близкой родственнице Е. Coli Clebsiella не нужен даже аммоний: в бескислородной среде кишечника она может синтезировать его из молекулярного азота атмосферы (в тканях человека и содержимом кишечника немало растворенного N2).
Из этих "диких" штаммов генетики вывели "капризные" штаммы, которые не могут синтезировать необходимые им вещества из аминокислот или витаминов; чтобы они росли, в среду следует добавлять нужное соединение. Такие мутанты-"неженки" называют ауксотрофами. Исследуя их, можно установить, сколько генов участвует в синтезе какого-либо соединения (синтез гистидина, например, контролируют десять генов).
Не менее важные признаки - устойчивость к антибиотикам, способность использовать в качестве источника энергии разные вещества, подвижность, патогенность, наконец, форма колонии на твердой среде.
Поставим такой опыт. Проведем конъюгацию клеток двух штаммов: ауксотрофного (акцептор) и "дикого", прототрофного (донор). Получив от донора неповрежденный ген, клетка акцептора вновь обретает утерянную способность, в частности, сбраживать молочный сахар-лактозу. Ограничив время конъюгации, можно довольно точно определить, в каком месте хромосомы этот ген находится (за единицу расстояния обычно принимают 1 минуту времени вхождения "мужской" хромосомы в "женскую"). Сейчас длину генов измеряют в тысячах нуклеотидных пар ДНК.
Так построили первые карты бактериальных хромосом. Оказалось, что единственная бактериальная хромосома не имеет ни начала, ни конца. Это замкнутая, кольцевая молекула ДНК с длиной окружности около 0,2 см (естественно, это кольцо многократно скручено: иначе оно просто не уместится в клетке микронных размеров).
На рисунке 21 дан фрагмент генетической карты хромосомы кишечной палочки штамма К12, полученной одной из первых. Символами показаны разные гены: Arg А - первый по счету ген, обусловливающий способность к синтезу аргинина; Аrа - способность сбраживать углевод арабинозу; Sm - устойчивость к антибиотику стрептомицину и т. д.
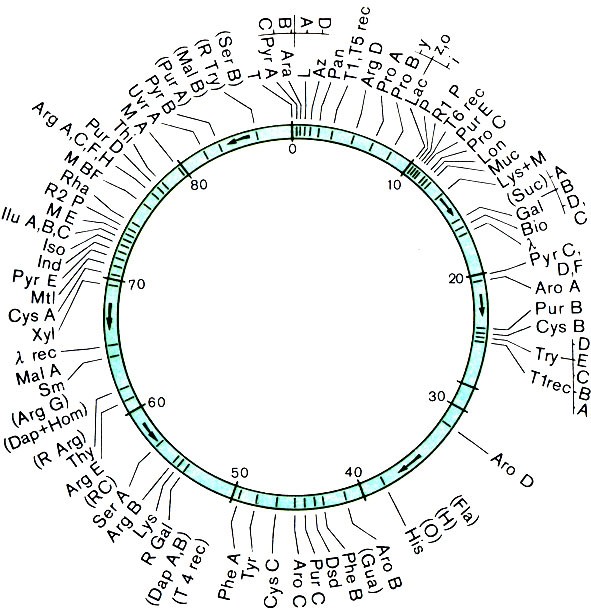
Рис. 21. Карта кольцевой хромосомы кишечной палочки
Зададимся вопросом: что определяет "пол" у бактерий, почему одна из них оказывается донором, а другая акцептором? У человека, например, мужской пол определяет Y-хромосома, вторая Х-хромосома в женском наборе остается неактивной. Нет ли чего похожего у конъюгирующих бактерий?
Оказалось, что не менее 90% всех известных штаммов кишечной палочки - акцепторы, остальные - доноры. Способность к донорству может исчезнуть, если подействовать на клетки донорского штамма ультрафиолетом или мутагенами, например акридиновыми красителями. Наконец, способность к донорству можно передать от клетки к клетке, превратить акцептора в донора. Следовательно, в донорских клетках есть какой-то материальный объект, содержащий ДНК (или состоящий из ДНК), который и отвечает за передачу генетической информации. Он образует мостик, по которому ДНК из одной клетки переходит в другую, может сам перейти по тому же мостику в клетку акцептора, придав ему донорские свойства, и может сам мутировать, как хромосома. Его назвали фактором F. Казалось, это аналог Y-хромосомы у мужчин. Однако схожесть была лишь внешняя.
Чтобы понять, что такое фактор F, вернемся в 1915- 1917 гг., когда были открыты вирусы бактерий - бактериофаги (или просто фаги).
Бактерии и вирусы. В 1915 г. канадский француз Ф. Д.'Эррель обнаружил у саранчи заразное заболевание - понос, приводящий к гибели насекомого. Его вызывали бактерии - коккобациллы. Размножая вновь открытую бактерию на среде с твердым агаром, Д'Эррель столкнулся с любопытным явлением: во многих чашках Петри на поверхности агара, заросшей слоем бактерий, появлялись мелкие прозрачные пятна - места, в которых бактерии погибли (теперь их называют бляшками). А в жидких средах культуры вдруг погибали, бактериальные клетки распадались, лизировались.
Такие случаи наблюдали и другие микробиологи, но лишь Д'Эррель догадался, что имеет дело с вирусом - паразитом бактерий и что он открыл паразита саранчи и паразита этого паразита! Он же первый предложил термин "бактериофаг" - пожиратель бактерий.
Очень быстро выяснилось, что фаги широко распространены. Д'Эррель обнаружил их у дизентерийной палочки, а потом их нашли практически у всех микроорганизмов, вызывающих самые разнообразные болезни - от чумы до скарлатины. Возникла идея фаговой терапии - лечение болезней фагами, имевшая большой успех в 20-х годах.
К огорчению врачей, оказалось, что многие фаги, убивая одни клетки бактерий, оставляют живыми другие клетки того же штамма, которые продолжают делать свое "черное" дело. Причина этого загадочного явления стала понятной лишь в конце 40-х годов благодаря блестящим работам знаменитого французского биохимика Андрэ Львова. А. Львов родился и вырос во Франции, но его родители русские. Отец ученого был политическим эмигрантом, осевшим во Франции до Октябрьской революции, а мать известна каждому из нас: она изображена на картине В. Серова "Девушка, освещенная солнцем".
Отметим, что бактериофаг - это ДНК (значительно реже встречаются РНК-содержащие фаги), заключенная в капсулу из белковых молекул. Попадая в бактерию (у сложных фагов есть очень хитроумные устройства, с помощью которых они "впрыскивают" в хозяйскую клетку свою ДНК; см. рис. 20), ДНК фага начинает "подрывную деятельность": выключает синтез хозяйских белков, синтезирует свои иРНК; на них как на матрицах рибосомы хозяина синтезируют фаговые белки. Сама фаговая ДНК активно реплицируется в клетке-хозяине. ДНК фагов либо кольцевая, либо становится кольцевой, попадая в бактериальную клетку. Далее ДНК встраивается в фаговые частицы, которые в большом числе накапливаются в клетке-хозяине и в конце концов разрушают ее.
А. Львов установил, что в части клеток, заражаемых некоторыми фагами, фаговая ДНК не образует фаговых частиц, а вместо этого встраивается в хромосому хозяина. Фаговая ДНК, или, как говорят, геном фага, реплицируется в составе хромосомы бактерии и вместе с ней передается из поколения в поколение. Встроенная фаговая ДНК направляет синтез только одного белка-репрессора, который не позволяет ей выйти из генома хозяина. Этот же белок не позволяет другим фаговым ДНК, попадающим в бактериальные клетки, хозяйничать в них. Таким образом, бактерии, в геном которых встроена фаговая ДНК, устойчивы (иммунны) к воздействию такого же фага, что и является зачастую причиной нечувствительности болезнетворных бактерий к бактериофагам. Это явление широко распространено в мире паразитов. Например, человек, имеющий в своем кишечнике солитера, не заражается его личинками повторно. Солитер всегда один - потому он и называется солитером ("одиноким").
Если же белок-репрессор разрушить (это происходит, в частности, при облучении клетки ультрафиолетовым светом), то фаговая ДНК выходит из генома хозяина и ведет себя в клетке так, словно попала в нее извне, т. е. в конце концов лизирует клетку. Фаги, способные встраиваться в геном хозяина, носят название лизогенных (их называют, кроме того, умеренными, так как они не всегда убивают клетку), а про клетку, которая в своем геноме несет такой фаг, говорят, что она находится в лизогенном состоянии.
Изучению умеренных фагов посвящено множество работ, и некоторые из них имеют самое непосредственное отношение к возникновению генной инженерии.
Чудесные ферменты - рестриктазы. Давно замечено, что наиболее детально исследованный из умеренных фагов - бактериофаг λ, паразитирующий в клетках штамма К кишечной палочки и выделенный после лизиса этих клеток, может лишь с очень низкой эффективностью заражать клетки другого штамма этой бактерии - штамма В. И только те немногие фаговые частицы, которые выжили в штамме В, охотно паразитировали в клетках этого штамма, но зато теряли способность заражать штамм К. Эти штаммы представляют собой два очень близких варианта кишечной палочки. Пытаясь выяснить причины столь странного поведения фага λ, ученые открыли чрезвычайно важное явление - рестрикцию-модификацию ДНК в клетках бактерий. Вот в чем суть названного явления.
В клетках кишечной палочки постоянно образуются ферменты - эндонуклеазы, которые узнают в молекулах ДНК строго определенные последовательности и разрезают ее двойную спираль в этих местах. Позже мы расскажем более подробно, как это происходит. Эндонуклеазы (теперь они широко известны под названием эндонуклеаз рестрикции или просто рестриктаз) и разрушали ДНК фага λ в штамме В кишечной палочки. Но тогда возникают вопросы: что в штамме К вообще нет рестриктаз? Почему рестриктазы в штамме В не разрушают свою собственную ДНК, а заодно и ДНК фага, который на них паразитирует?
Оказалось, что в штамме К рестриктазы есть, но иные: они расщепляют ДНК по другим участкам. Более того, в клетках штамма К есть фермент, который модифицирует (метилирует, присоединяет метильную группу СН3) основание в участке ДНК, узнаваемом рестриктазой этого штамма, и делает его для нее недоступным, т. е., попросту говоря, защищает ее ДНК от своих рестриктаз. Вся ДНК, которая синтезируется в бактериальной клетке, подвергается защите уже в момент своего образования. Когда же в клетку попадает чужеродная незащищенная метилированием ДНК, рестриктазы расщепляют ее на куски, которые станут "жертвой" других, уже менее специфичных нуклеаз. И лишь те молекулы чужеродной ДНК, которые успевают модифицироваться ферментами модификации, могут в этих клетках функционировать. Вот почему небольшой части ДНК фага л из штамма К удается спастись в штамме В. Их спасают "забежавшие вперед" ферменты - метилазы хозяйской клетки.
Сейчас известно уже несколько сотен различных рестриктаз из множества бактерий. Если вы внимательно ознакомитесь с рисунком 22, в котором приведены наиболее широко употребляемые рестриктазы, то увидите, что они отличаются друг от друга не только нуклеотидными последовательностями, по которым они расщепляют ДНК, но и по способу действия. Одни рестриктазы образуют однотяжевые участки длиной в четыре нуклеотидных остатка, другие - в два остатка, третьи разрезают ДНК так, что однотяжевых участков вообще не возникает. И самое важное: участки узнавания ДНК многими рестриктазами обладают симметрией второго порядка. Что это такое? Рассмотрим участок ДНК, узнаваемый и разрезаемый одной из рестриктаз кишечной палочки, известной под названием Eco RI (см. рис. 22).
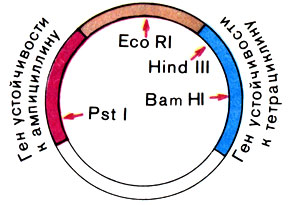
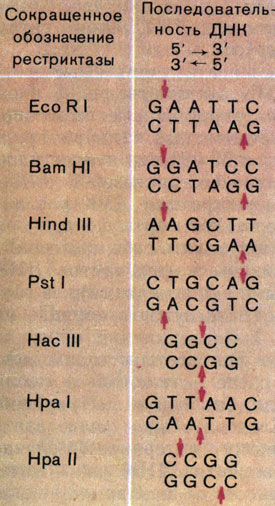
Рис. 22. Плазмида pBR 322. Показаны уникальные места разрезания ДНК рестриктазами. Слева приведена таблица наиболее широко применяемых рестриктаз и последовательности ДНК, ими расщепляемые (стрелками показаны места разрыва цепей). Сокращения рестриктаз даются по латинским названиям микроорганизмов, из которых выделена рестриктаза. Так, EcoRI означает: рестриктаза выделена из кишечной палочки (Ecsherichia coli) штамма R первой по счету
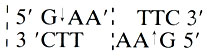
Если в центре этой шестичленной последовательности мысленно провести ось (перпендикулярно плоскости листа), а затем повернуть эту последовательность на 180° в плоскости чертежа, то получим ту же нуклеотидную последовательность. Иными словами, нуклеотидный текст, записанный в этой последовательности, можно читать как слева направо, так и справа налево (помня только об асимметричности межнуклеотидных связей), и он будет одним и тем же. В лингвистике такие тексты называют перевертышами ("А роза упала на лапу Азора"). И еще одна очень важная особенность разрыва, генерируемого в ДНК рестриктазами: образующиеся на концах однотяжевые последовательности ДНК комплементарны друг другу; их образно называют "липкими" концами, с их помощью фрагменты ДНК можно снова соединить (слепить) друг с другом.
Нуклеотидные последовательности, узнаваемые рестриктазами, встречаются в ДНК достаточно редко. При этом шестичленные участки узнавания, естественно, встречаются реже, чем четырехчленные (например, в ДНК бактериофага Т7 длиной в 35 000 пар нуклеотидов нет ни одного участка узнавания рестриктазой Eco RI). Это позволяет строить карты рестрикции ДНК различных вирусов и фагов. Пример такой карты показан на рисунке 22. Нужно только представлять себе, как удается разделить такую сложную смесь фрагментов ДНК (называемых рестрикционными фрагментами), а затем расположить эти фрагменты в нужном порядке на карте.
Разделяют рестрикционные фрагменты методом электрофореза в студнеобразной среде - геле. Как и любая другая кислота, ДНК в среде, близкой к нейтральной, заряжена отрицательно. Следовательно, если взять пластинку, сделанную из пористого материала (в случае крупных рестрикционных фрагментов ДНК таким материалом служит гель из природного полисахарида - агарозы), пропитанную раствором электролита, на один из концов пластинки нанести раствор ДНК, поместить эту пластинку между двумя электродами и приложить к ним разность потенциалов так, чтобы положительный электрод находился на удаленном от образца ДНК конце пластинки, то молекулы ДНК будут двигаться в направлении от катода к аноду (от - к +). Так как в процессе электрофореза макромолекулам ДНК приходится преодолевать сопротивление, которое создает полимерная сетка геля (образно говоря, протискиваться сквозь ячейки в сетке геля), то чем крупнее фрагмент ДНК, тем медленнее он будет двигаться. В конце концов все фрагменты ДНК распределятся на пластинке с агарозным гелем в соответствии с их длиной. Их можно увидеть, например, в виде яркосветящихся, флуоресцирующих в невидимом ультрафиолетовом свете полос, если в электролит перед электрофорезом добавить краситель бромистый этидий, который образует с ДНК флуоресцирующие комплексы. Изменяя в геле концентрацию агарозы, можно придавать ему разную плотность - от полужидкого до твердого, как мармелад (это лакомство как раз и делают на основе агароз), и, следовательно, разделять фрагменты ДНК желаемой длины.
Для того чтобы узнать последовательность расположения фрагментов ДНК, надо изучить порядок появления фрагментов в ходе частичного расщепления рестриктазой. Например, если в простейшем случае ДНК расщепляется рестриктазой на три фрагмента - А, В и С, а при неполном гидролизе этой ДНК той же рестриктазой получается более длинный фрагмент, который при дальнейшем расщеплении дает фрагменты А и В, то порядок фрагментов именно такой, как на рисунке 22. Так получают карты генов, называемые рестрикционными. Как вы увидите дальше, они совершенно необходимы генным инженерам в их практической работе.
Первыми догадались применить рестриктазы для получения индивидуальных генов Стэнли Коен из Стэнфордского университета и его коллега из Калифорнийского университета (США) Герберт Бойер в 1972 г. К этому времени эти ученые были уже хорошо известны благодаря своим работам по плазмидам бактерий.
Плазмиды - дар природы генным инженерам и проклятие врачей. Плазмиды - кольцевые молекулы ДНК, размером от 2-3 до нескольких десятков тысяч пар оснований. Они существуют и реплицируются независимо от хромосомы бактерии, хотя и используют для этого тот же самый ферментативный аппарат клетки. Плазмиды, как и некоторые умеренные фаги, - одни из главных "героев" этой книги, а почему - вы скоро узнаете.
Многие плазмиды могут передаваться от одной бактерии к другой при конъюгации. Их называют трансмиссивными (трансмиссия - передача, перенос). У всех трансмиссивных плазмид имеются гены, отвечающие за синтез особого белка - пилина. Именно этот белок слагает трубочки (ворсинки - пили), по которым ДНК при конъюгации переходит из клетки в клетку. Но то же делает и половой фактор: F - фактор бактерий. Не плазмидой ли он является? Действительно, это трансмиссивная плазмида, специализирующаяся на переносе хозяйских генов. И "мужские" клетки-доноры - это просто клетки-акцепторы, зараженные такой плазмидой (теперь, кроме фактора F, описаны и другие плазмиды, оказывающие хозяевам такие же "услуги").
Генетики быстро разобрались и в том, как происходит генетическая рекомбинация у бактерий при конъюгации. Старая хромосома и новая, перетекшая в клетку через пилиновую трубочку, построенную фактором F, образуют комплекс - две нити ДНК соединяются гомологичными местами. Обычно гаплоидная, однохромосомная, клетка бактерии на какое-то время становится диплоидной. Далее происходит процесс, очень похожий на кроссинговер у высших, ядерных, организмов. Лежащие рядом хромосомы обмениваются генами и группами генов. А затем при делении клеток хромосомы расходятся, бактерии снова становятся гаплоидными - до очередной конъюгации.
Теперь перейдем к явлению трансдукции (переноса). Как вы помните, для передачи генетической информации у бактерий требуется или наличие лизированных клеток, т. е. свободной ДНК (трансформация), или физический контакт клеток при половом процессе. При трансдукции не требуется ни того ни другого.
Дж. Ледерберг, открывший "пол" у бактерий, поставил изящный опыт. Он взял U-образную трубку, оба колена которой разделялись фильтром из пористого стекла, - так называемую трубку Дэвиса. Микробиологи ее применяют, когда изучают действие веществ, выделяемых одним микробом на развитие другого. Ведь микробы не проходят через узкие поры, а молекулы их метаболитов проходят. Но через них проходят и фаги.
В одно колено трубки наливали культуру ауксотрофных бактерий, не способных синтезировать какую-либо аминокислоту, а в другое - культуру "диких", автотрофных (иногда штаммы двух ауксотрофов, но разных, с разными генетическими дефектами). В конце опыта ауксотрофы приобретали способность синтезировать эту аминокислоту! Может быть, протейная палочка в опыте Л. А. Зильбера таким же образом приобрела признак сыпнотифозной: ведь их разделяла полупроницаемая мембрана?
Основное условие успеха опыта: штаммы должны быть заражены лизогенным (умеренным) фагом. Фаги могут переносить генетическую информацию (гены) от одной хозяйской клетки к другой.
Бактерии вместо типичного полового процесса, свойственного эукариотам, разработали иные способы рекомбинаций, не менее эффективные. Вы скажете: все это, конечно, очень любопытно, но что нам до обмена генов у бактерий, какое это может иметь практическое значение? Первостепенное, и примеры, которые мы приведем, убедят вас в этом.
Дифтерию сейчас научились успешно лечить, однако раньше она уносила немало жизней, особенно детских. Мало кто знает, что сама по себе дифтерийная палочка неопасна. Она вызывает лишь легкое ангиноподобное заболевание. Смертельно опасен лишь выделяемый ею яд - дифтерийный токсин, вызывающий общее отравление организма. Это токсин белковой природы, а ген, определяющий его синтез, находится в плазмиде дифтерийной палочки!
Другой не менее опасный для человека токсин - холерный, выделяемый холерным вибрионом. Описан случай вспышки холероподобного заболевания, при котором вибрионы не были обнаружены. Оказалось, что ген холерного токсина в результате трансдукции или трансформации попал в вездесущую кишечную палочку.
Когда в практику медицины вошли антибиотики, врачи были убеждены, что наступила золотая эра медицины, что все бактериальные болезни будут побеждены. Высказывались, в частности, утверждения, что в наши дни можно было бы вылечить Пушкина, тяжело раненного на дуэли. Сшить поврежденный пулей кишечник врачи могли и тогда, но смертельный сепсис (заражение крови) был бы неизбежен. Вот если бы в распоряжении врачей, лечивших Пушкина, имелся пенициллин! Увы, сейчас медики вряд ли будут утверждать так решительно. Бактерии приспосабливаются к антибиотикам так же легко, как и к фагам. Причина - жесточайший отбор устойчивых к антибиотику бактерий.
Задумались ли вы, почему плесневые грибки, бактерии и другие микроорганизмы синтезируют лекарства для человека? Оказалось, что антибиотики имеют много родственных соединений, участвующих в обмене веществ у микробов. Часто соединение, безвредное для одного микроорганизма, для другого ядовито - и обладатель его вытесняет из питательной среды конкурентов. Пенициллин открыл английский ученый А. Флеминг, подметивший, что вокруг колоний плесени рода Penicillium образуется стерильная, свободная от бактерий зона. Стенка клетки бактерий слагается из длинных цепочек азотсодержащих полисахаридов - ацетилглюкозамина и ацетилмурамовой кислоты, сшитых короткими цепочками аминокислотных остатков - пептидами. В этих пептидах необычные формы аминокислот: глутаминовая кислота правая, а аланин и правый, и левый. Поэтому оболочки бактериальных клеток не расщепляются обычными ферментами - протеазами.
Пенициллин как раз блокирует рост этих пептидных мостиков, клеточная стенка не растягивается, и бактерия лопается. А так как пенициллин практически нетоксичен для эукариот, он и получил распространение как лекарство. Лишь те бактерии, которые в результате отбора тем же пенициллином "научились" расщеплять его, не боятся высоких концентраций антибиотика. Другие антибиотики действуют на бактерии по- иному; левомицетин, например, подавляет у них синтез белка; стрептомицин искажает течение белкового синтеза на рибосомах, в белок включаются не те аминокислоты, которые нужны, и продукт синтеза оказывается дефектным.
По-разному бактерии приспосабливаются к ним. Порой антибиотик не расщепляется, а модифицируется каким-нибудь ферментом - достаточно иногда присоединения или отщепления метильной группы, чтобы он потерял свои полезные для человека свойства. При чем же тут плазмиды? - спросите вы. Дело в том, что гены, кодирующие ферменты, расщепляющие или модифицирующие антибиотики (пенициллин и тетрациклин, стрептомицин и левомицитин), могут переноситься от бактерии к бактерии вирусами и плазмидами. Устойчивость к антибиотикам может передаваться в мире микробов, не считаясь с видовыми границами. Ведь у кишечной и чумной палочки есть общие трансмиссивные плазмиды.
Мрачную известность получили в последнее время устойчивые ко многим антибиотикам штаммы золотистого стафилококка - причина многих послеоперационных осложнений. Единственное эффективное средство против него - антистафилококковый гаммаглобулин, т. е. антитело на оболочечные антигены этого микроба. К сожалению, пока он выделяется из донорской крови и потому малодоступен.
Мы привели лишь очень немногие факты, показывающие, почему надо изучать взаимоотношения вирусов, плазмид и бактерий.
Встает вопрос: как выделять плазмидную ДНК в чистом виде? Несколько способов получения чистых плазмид уже разработано. Опишем самый распространенный.
Сначала во взвесь бактериальных клеток добавляют вещества, разрушающие их оболочки. Клетки разрушаются, лизируются, и ДНК переходит в раствор. Лизис виден невооруженным глазом: мутная легкоподвижная жидкость превращается в прозрачную, вязкую. Получается смесь бактериальной ДНК и плазмидной, но судьбы их разные. Кольцевые хромосомы бактерий огромны, и получить их целыми очень сложно: они ломаются на линейные фрагменты.
Иное дело - плазмидная ДНК или ДНК умеренных фагов. Ее кольца много меньше, чем у бактерий; у самых малых плазмид молекулярная масса всего около 2,5 млн. дальтон. К тому же они компактно уложены (суперскручены) и имеют все шансы сохраниться целыми. Как разделить смесь линейной ДНК бактерии и кольцевой (плазмиды)? Сейчас чаще всего используют центрифугирование в градиенте концентрации тяжелой соли, например хлористого цезия. В раствор ДНК добавляют CsCl и откручивают на центрифуге при высоких скоростях - до ускорения, в 105 тыс. превышающего нормальное земное. В таких условиях создается градиент концентрации CsCl, которая уменьшается от дна пробирки к поверхности. В этом градиенте молекулы ДНК всплывают или тонут, пока не остановятся в слое с равной плотностью. Так, воздушный шарик, заполненный водородом, взлетает к разреженным слоям атмосферы, пока не уравновесится. Нагрузите его побольше - он остановится на меньшей высоте, а то и не взлетит.
То же происходит и с молекулами. Тяжелая, плотная РНК "проваливается" на дно пробирки. Легкие белки образуют слой под мениском. А ДНК образует полосы, располагаясь слоями по удельной плотности.
Если бактериальная и плазмидная ДНК по этому признаку отличаются, разделить их легко. Если же не различаются, разделить смесь очень нелегко. На помощь приходит светящийся в ультрафиолетовых лучах краситель - бромистый этидий, или этидий бромид - ЭБ. ЭБ встраивается в полинуклеотидные цепи между основаниями, несколько раздвигая их. Молекула нуклеиновой кислоты в комплексе с ЭБ удлиняется, а плотность ее уменьшается. Линейные фрагменты ДНК можно насыщать ЭБ до предела. Иное дело - кольцевые молекулы. Сначала они переходят из сверхскрученного состояния в правильное кольцо. Такое кольцо называют релаксированным. Релаксированная кольцевая ДНК неохотно связывается с ЭБ. Так возникает разница в удельных плотностях. В ультрафиолете через полупрозрачную стенку пластиковой пробирки видны две светящиеся оранжевым светом полоски: тонкий слой плазмидной ДНК и широкий - хромосомной. Каждую из них можно отсосать отдельно, проколов иглой шприца стенку пробирки. ЭБ хорошо отделяется от ДНК спиртом (ДНК выпадает в осадок, а ЭБ остается в растворе) .
Это очень распространенный способ, хотя есть и другие. Он привлекателен еще и тем, что исследователь видит материал, с которым работает, невооруженным глазом, что бывает в молекулярной биологии и генной инженерии нечасто.
Раньше генетики предсказывали устройство плазмидных и фаговых ДНК только экспериментально, не видя их; теперь они могли видеть отдельные кольца в электронном микроскопе и работать с генами как с химическими веществами.
В свою очередь, генетика микроорганизмов принесла будущей генной инженерии неоценимый дар - селективные среды.
Селекция означает отбор. Иногда в популярной литературе можно встретить такое утверждение. Раньше, мол, генетики только отбирали случайные изменения генов, а мы теперь направленно тасуем гены, и отбор нам не нужен. Запомните: такое утверждение безграмотно. Наоборот, в генетике бактерий и генной инженерии понятие искусственного отбора обрело новую жизнь. Ведь все события, о которых мы рассказали в этой главе, будь то трансформация или трансдукция, происходят с низкой частотой. Как найти редкое генетическое событие? Только отобрав его из массы ненужных. А отбор эффективен, когда есть из чего отбирать. В массовой популяции можно обнаружить редчайший вариант.
Обычная концентрация бактерий - миллион клеток в миллилитре. А отбор проводят селективные среды.
Первым селективную среду использовал С. Н. Виноградский в 1894 г. в поисках свободноживущего микроорганизма, усваивающего молекулярный атмосферный азот. Обычно микробиологи выращивают колонии бактерий и грибков на питательных средах, содержащих агар (азотсодержащий полисахарид, получаемый из водорослей) или желатину. Несколько капель материнской культуры размазывают шпателем по поверхности твердой среды и помещают в термостат. На тех местах, куда попали клетки, способные расти на такой среде, вырастают колонии, каждая из которых - потомство одной исходной клетки.
С. Н. Виноградский вместо агара или желатины применил гель кремниевой кислоты, иначе говоря, затвердевший силикатный клей Na2SiO3 с добавками сахаров и солей, но без азота. Поэтому любая колония, выросшая на такой среде, автоматически оказывалась азотфиксирующей: ведь необходимый для жизни азот она могла получить только из воздуха.
Метод селективных сред оказался очень эффективным. Продемонстрируем лишь несколько примеров его успешного применения.
Дана задача: из многих миллиардов клеток "дикой", автотрофной бактерии отобрать те, которые потеряли способность синтезировать незаменимую аминокислоту гистидин. С этой целью культуру бактерий выращивают в жидкой среде без гистидина, но с высокой концентрацией антибиотика пенициллина. Те клетки, которым гистидин не нужен, начинают расти: тут же оболочки их лопаются и бактерии погибают. Ведь пенициллин останавливает рост их оболочек, и увеличивающаяся в объеме цитоплазма разрывает клетку. Нуждающиеся в гистидине ауксотрофы остаются живы - они без него не растут. Остается осадить культуру в центрифуге, отмыть от пенициллина чистой средой и пересеять на твердую среду, содержащую гистидин. Таким способом можно отобрать одну нужную бактерию из сотен миллионов и за сутки получить от нее многомиллионное потомство.
Еще проще получить выращиванием на агаре с антибиотиком культуру бактерий, к этому антибиотику устойчивых. Когда в Японии обнаружили возбудителя ангины, устойчивого к стрептомицину, генетики бактерий, заинтересовавшись этим фактом, получили штаммы ангинового стрептококка, для роста которых стрептомицин был необходим. Так у Стругацких ("Понедельник начинается в субботу") Модест Матвеевич Камноедов, борясь с нетопырями в вестибюле института, вывел породу, питающуюся пиретрумом, смешанным с хлорофосом.
Работа с плазмидами очень облегчается тем, что многие из них содержат гены, обеспечивающие хозяйским клеткам устойчивость к антибиотикам. Раньше их называли R-факторами (от английского resistance - устойчивость). Допустим, нам нужно заразить какую-нибудь культуру плазмидой и отобрать зараженные клетки. Проинкубируем взвесь нужных бактерий с этой плазмидной ДНК и сделаем посев на селективной среде с антибиотиками. Известно, что плазмида имеет ген устойчивости. Значит, только зараженные ею клетки прорастут в колонии на ядовитом агаре, остальные погибнут.
Некоторые плазмиды содержат гены таких ферментов, которые позволяют хозяйским клеткам усваивать в качестве источника вещества и энергии новый, непривычный субстрат, например фенол или нефтяные углеводороды. Генетики микроорганизмов недавно вывели любопытный штамм бактерии из рода Псевдомонас. Клетки его содержат сразу несколько таких плазмид, что им позволяет усваивать все основные компоненты нефтяного загрязнения. Этой бактерии придается важное значение в охране окружающей среды.
Успехи практического применения генетики микробов стали особенно значительными в последние 30 лет. У многих людей стали возникать заманчивые идеи, суть которых можно свести к следующему. Пока генетическая рекомбинация у бактерий приносит человеку больше вреда, чем пользы. Достаточно вспомнить устойчивость к антибиотикам, которая в мире микробов распространяется как эпидемия. Но теперь, когда мы знаем механизм действия плазмид умеренных фагов, что мешает заставить бактерию, ту же кишечную палочку, синтезировать в культуре нужный нам белок, например какой-нибудь человеческий гормон или фермент?
Уже есть система для переноса кусочка ДНК в клетку - плазмида или умеренный вирус. Эти трансмиссивные кольцевые молекулы ДНК назвали векторами. Есть фермент, который "пришьет" нужный ген к молекуле-вектору (ДНК-лигаза). И пусть этот акт переноса генетической информации происходит с ничтожной частотой - волшебные селективные среды позволяют нам его выявить. Остается научиться получать фрагменты ДНК с нужной нуклеотидной последовательностью. И тут С. Коен и Г. Бойер, о которых мы уже говорили, одни из первых вспомнили о рестриктазах. Именно эти ферменты, расщепляющие ДНК в заданном месте, проложили последний участок дороги, ведущий к власти над геном.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'