
§ IV.3. Комплементарное узнавание оснований (экспериментальные данные)
IV.3.1. Образование одиночной пары. Комплементарное инструктирование основано на том, что пары образуются только между А и У или между Г и Ц соответственно. Что же лежит в основе такого специфичного взаимодействия, которое гарантирует точное считывание, трансляцию и усиление генетических сообщений во всем органическом мире, от фага до человека?
Биохимик ответил бы, конечно: "Специфичные ферменты", физико-химик, возможно, предпочел бы сказать: "Специфичные силы". Правы и тот и другой, потому что мы достаточно хорошо знаем некоторые ферменты, но мы знаем также, что существует специфичное взаимодействие без участия ферментов, например гибридизация комплементарных цепей нуклеиновых кислот.
Структуры специфичных комплементарных пар, предложенные Ф. Криком и Дж. Уотсоном в их эпохальной статье [1], показаны на рис. 8. Однако, взглянув на рис. 9, можно немедленно убедиться в том, что одних только водородных связей недостаточно для объяснения очевидного выбора природы.
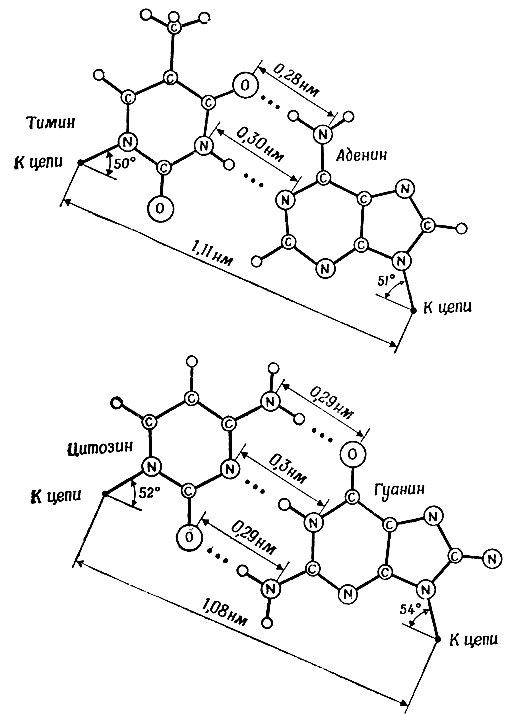
Рис. 8. Комплементарные пары оснований
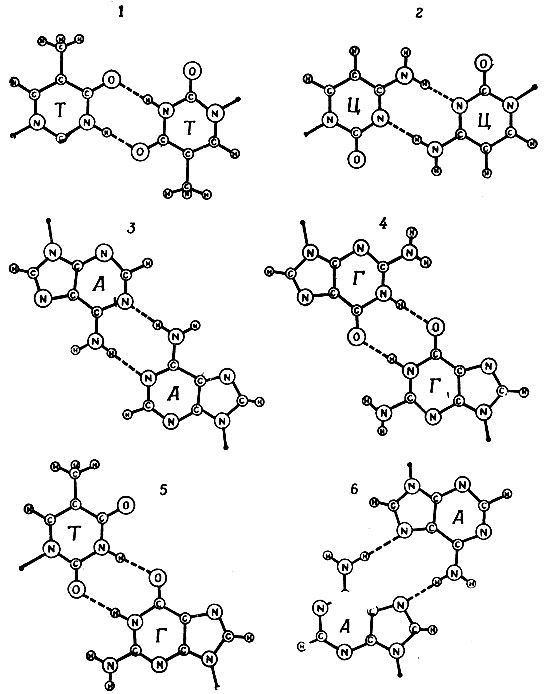
Рис. 9. 'Некомплементарные' комбинации оснований
Во-первых, существует различие в геометрии разных пар (рис. 9), так что изоморфизм двух уотсон-криковских пар определенно будет давать преимущество в отношении образования однородных двухцепочечных структур, содержащих все четыре нуклеотида, и особенно в отношении эволюционной адаптации общего полимеризующего фермента. С другой стороны, существует возможность того, что эволюция началась с двухбуквенного кода, содержащего, например, только А и У. Наконец, до того как ферменты приобрели специфическую адаптацию, возможно, существовал какой-то тип взаимодействия кодон - антикодон с "комплементарностью" по иным параметрам. Для того чтобы ответить на эти вопросы, необходимы соответствующие эксперименты.
Некоторые такие эксперименты уже проделаны. Например, имеются количественные данные о свободных энергиях образования одиночной пары для различных комбинаций оснований. Попытки провести такие измерения, пользуясь в качестве растворителя водной средой, окончились разочарованием: оказалось, что ни одна из пар не стабильна. Даже при самых высоких концентрациях довольно хорошо растворимых нуклеотидов нельзя было заметить образования одиночных пар. И мы знаем почему: если водородные связи между такими полярными группами, как NH, NH2, ОН и СО или N, являются единственным источником стабилизации, то полярные молекулы Н2O будут слишком сильно с ними конкурировать, сольватируя все доступные дипольные группы. Следовательно, для опытов, где исследуется относительная устойчивость, лучше пользоваться неполярным растворителем.
Проведены измерения в различных неполярных растворителях с нуклеозидами, которые становятся растворимыми в этих растворителях при замещении различных положений в рибозе неполярными группами (это не мешает основаниям образовывать водородные связи). Очень большая работа в этом направлении, в частности изучение инфракрасных спектров различных замещенных нуклеозидов, проведена А. Ричем и его сотр. [76, 77] в Массачусетском технологическом институте. Аналогичную работу опубликовали Э. Кюхлер и И. Деркош из Венского университета [78]. Диэлектрические измерения образования пар были проведены Т. Функом в нашей лаборатории [79], частично в сотрудничестве с Р. Хопманом и Ф. Эггерсом. Они определили также кинетические параметры по данным релаксационных измерений [80].
Все эти результаты в общем согласуются друг с другом. Комплементарные пары АУ и ГЦ самые сильные по сравнению с другими альтернативами. В табл. 12 приведены некоторые значения констант стабильности, определенные по данным диэлектрических измерений.
Можно видеть, что пара АУ по крайней мере в десять раз более стабильна, чем АА или УУ, тогда как ГЦ является самой прочной парой среди всех комбинаций, содержащих Г или Ц. Пара ГЦ гораздо стабильнее, чем пара АУ. Поскольку Г обнаруживает также значительное "самоспаривание", то определение констант стабильности любых гетеропар, содержащих гуанин, за исключением пары ГЦ, становится невозможным. Следует отметить, что некоторые пары могут образоваться разными способами и что константы равновесия, приведенные в табл. 12, представляют собой суммарные значения.
![Таблица 12. Константы стабильности для спаривания. Kass [M-1] при 25°С (2'-3'-5'-0 - замещенные рибонуклеозиды в неполярных средах)](pic/000367.jpg)
Таблица 12. Константы стабильности для спаривания. Kass [M-1] при 25°С (2'-3'-5'-0 - замещенные рибонуклеозиды в неполярных средах)
Все пары образуются очень быстро. Константы скорости показывают, что каждое столкновение ведет к образованию пары и что времена жизни пар в общем меньше одной микросекунды.
Относительно большая устойчивость пар АУ и ГЦ, вероятно, обусловлена одной сильно поляризованной водородной связью. Единственная комбинация ХН ... Y такого типа, общая для пар АУ и ГЦ, но отсутствующая у их конкурентов, - это водородная связь между довольно кислой группой NH(pK ∼ 9,5) и азотом кольца (рK ∼ 4,5). Большую стабильность такой связи можно объяснить на основе квантовой механики. Итак, эта важная предпосылка возникновения кода в принципе объясняется физической теорией.
В итоге можно сказать, что, судя по всем имеющимся данным, пары образуют преимущественно те основания, которые мы теперь называем "комплементарными". "Узнавание" - процесс очень быстрый, но вследствие этой быстроты абсолютные стабильности очень низки - так низки, что в полярных средах ощутимого образования пар не происходит. Такие низкие стабильности не могут обеспечить очень точное узнавание, необходимое для чтения кода в длинных последовательностях. Для того чтобы получить больше информации об узнавании оснований при последовательном считывании кода, следует изучить кооперативные взаимодействия в олигомерах и полимерах.
IV.3.2. Кооперативные взаимодействия в олиго- и полинуклеотидах. Мы уже подчеркивали, что в водных средах отдельные пары оснований слишком нестабильны, чтобы их можно было обнаружить современными методами. С другой стороны, хорошо известно, что комплементарные полимерные цепи образуют очень устойчивые двойные спирали, которые "плавятся" только при высоких температурах. Форма кривых плавления указывает на сильное кооперативное поведение. Источник кооперативности - относительно сильное стопочное взаимодействие между соседними парами оснований, а также хелатные эффекты, возникающие вследствие "замораживания" степеней свободы после образования спирали. Очевидно, что эти кооперативные эффекты сильно увеличивают "инструктивные" способности нуклеиновых кислот.
Прямой путь исследования кооперативных явлений - строить полимер шаг за шагом, начиная с мононуклеотида, и изучать, как изменяются его термодинамические и кинетические свойства с увеличением длины цепи. Большим преимуществом является относительная простота термодинамического и кинетического анализа конформационных изменений олигомеров, особенно то, что спаривание оснований происходит у них по типу "все или ничего". Трудности такой работы на олигомерах связаны с получением материала: приходится проводить расщепление полимерных образцов, а затем разделять, собирать и очищать продукты гидролиза. Различные группы в нашей, а также в других* лабораториях занимались этим в течение нескольких лет.
* (Например, Р. Болдуин (Стэнфорд), Д. Крозерс (Йель), Н. Дэвидсон (Пасадена), П. Доти (Гарвард), Дж. Фреско (Принстон), Б. Зимм (Ла Хойя))
Первые кинетические исследования были выполнены в дипломной работе Д. Пёршке [72, 73] на олигомерных адениловых кислотах (длина цепи от 2 до 10 мономеров). Как уже говорилось, олиго- и поли-рибо А образуют двуспиральные структуры в кислой области (pH ∼ 4), и это дало хорошую модель для наших первых исследований. Затем Д. Пёршке [82] изучил образование двойных и тройных спиралей из олиго-рибо А и олиго-рибо У при нейтральном pH (длина цепи до 18 мономеров). Эта работа включала в себя термодинамические (фазовые диаграммы и кривые плавления, которые регистрировались с помощью спектрофотометрии в ультрафиолете), а также кинетические исследования с использованием проточных и релаксационных (температурный скачок) методов.
Распространение этих исследований на ГЦ-олигомеры встретилось с большими трудностями, обусловленными агрегацией этих молекул до более сложных структур. С. Поддеру (во время его пребывания в Гёттингене) удалось исследовать спаривание тетрамеров

а также спаривание ГфГ и ГфГфГ с поли-рибо Ц.
Г. Маас и объединенная группа из лабораторий Гёттингена и Брауншвейг-Штокгейма (Д. Ризнер, Р. Рёмер, С. Коутс) в сотрудничестве с группой из лаборатории Х. Цахау в Мюнхене изучали термодинамику плавления и конформационную кинетику тРНК [84] (рис. 2) и ее фрагментов с известной последовательностью [85], которые они получали, расщепляя нативную молекулу в определенном положении по методу, описанному Х. Цахау [86].
Очень ценные данные о специфичном спаривании различных последовательностей получены в лаборатории П. Доти (Гарвардский университет) при исследовании олигомерных сополимеров [87, 88], таких, как
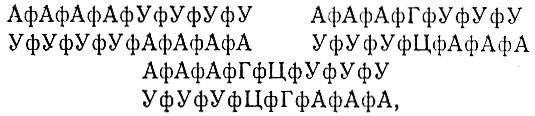
а также различных олигомеров, спаренных с открытыми комплементарными последовательностями тРНК (табл. 13).
![Таблица 13. Константы стабильности для спаривания триплетов и квадруплетов оснований (три- и тетрануклеотидов) с открытыми областями тРНК (преимущественно, антикодонами) [87, 88]](pic/000370.jpg)
Таблица 13. Константы стабильности для спаривания триплетов и квадруплетов оснований (три- и тетрануклеотидов) с открытыми областями тРНК (преимущественно, антикодонами) [87, 88]
1) (Kass(M-1) измерены в водном растворе (1,0 М NaCl, 10 мМ MgCl2, 10 мМ фосфатный буфер. pH 7) при 0°С. При значениях К < 400 М-1 ассоциация недостоверна. А.* - N (6) диметиладенин; У* - псевдоурацил (ψ); Г* - 2-О-метилгуанин; Ц* - 2-О-метилцитозин.)
2) (Личное сообщение О. Уленбека.)
Во время визитов в Гёттинген два сотрудника П. Доти - Ф. Мартин и О. Уленбек - проводили совместно с Д. Пёршке дальнейшие термодинамические и кинетические исследования упомянутых олигомеров [89]. Ниже приводятся результаты и (предварительные) выводы из всех этих работ.
Равновесие спираль - клубок. Кривые "плавления" двойных спиралей зависят от длины цепи: наклон кривых увеличивается с длиной цепи. График зависимости обратной "температуры плавления" (температуры полуперехода спираль → статистический клубок) от 1/(ν - 1) (ν - число единиц, отвечающее максимальному числу пар оснований в двухцепочечной спиральной структуре) представляет собой прямую линию. Наклон этой прямой пропорционален 1/ΔH; отрезок, отсекаемый ею на координатной оси, дает 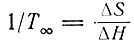 - величину, обратную температуре плавления "бесконечно длинной" спирали. "Бесконечно" означает: длинную по сравнению с "кооперативной длиной", в которую входит около 30 пар оснований. Следовательно, T∞ можно определить из опытов с длинными полинуклеотидами. Для того чтобы получить этот результат, необходимо ввести поправку на одноцепочечное стопочное взаимодействие, степень развития которого различна при разных температурах плавления (как можно определить из опытов с одноцепочечными полимерами). Когда длина цепи мала, можно считать, что переход от спирали к клубку происходит по закону "все или ничего". Пусть σis - константа стабильности для каждой пары оснований, примыкающей к непрерывной последовательности (i-1) пар. Тогда, помня, что "параметр нуклеации" σi близок к единице, если i больше некоторого числа n - "длины нуклеации", можно написать выражение для константы равновесия перехода типа "все или ничего", в котором участвует ν > n пар оснований:
- величину, обратную температуре плавления "бесконечно длинной" спирали. "Бесконечно" означает: длинную по сравнению с "кооперативной длиной", в которую входит около 30 пар оснований. Следовательно, T∞ можно определить из опытов с длинными полинуклеотидами. Для того чтобы получить этот результат, необходимо ввести поправку на одноцепочечное стопочное взаимодействие, степень развития которого различна при разных температурах плавления (как можно определить из опытов с одноцепочечными полимерами). Когда длина цепи мала, можно считать, что переход от спирали к клубку происходит по закону "все или ничего". Пусть σis - константа стабильности для каждой пары оснований, примыкающей к непрерывной последовательности (i-1) пар. Тогда, помня, что "параметр нуклеации" σi близок к единице, если i больше некоторого числа n - "длины нуклеации", можно написать выражение для константы равновесия перехода типа "все или ничего", в котором участвует ν > n пар оснований:
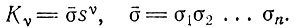 (IV.24)
(IV.24)Кинетические данные (см. ниже) показывают, что длина нуклеации n при комнатной температуре равна трем для АУ-спиралей и двум для ГЦ-спиралей при температурах выше 50°С. Это эквивалентно утверждению, что σn приближается к единице для n ≥ 3. Тогда кривые плавления показывают, что для n ≥ 3 имеется постоянный (и отрицательный) инкремент ΔHs и ΔSs, связанный с каждой парой оснований, причем
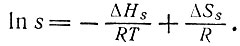 (IV.25)
(IV.25)Тот факт, что исправленная 1/Tm пропорциональна 1/(ν-1), а не 1/ν, показывает, что постоянный инкремент не имеет места для n ≤ 3, что, в частности, параметр нуклеации обнаруживает температурную зависимость, противоположную таковой для s, так что σ¯s почти не зависит от температуры (ΔHσs ∼ 0). Хотя σ¯s не является константой стабильности для первой пары оснований (она равна σ1s), физическая интерпретация состоит в том, что существенная часть ΔHs происходит за счет стопочного взаимодействия (отметим относительно большой инкремент ΔH, обусловленный стопочным взаимодействием, для каждой отдельной цепи), а не от образования водородных связей между комплементарными основаниями. Значение ΔH для первой пары оснований должно быть, таким образом, довольно мало. Эта пара очень нестабильна (σ1s < 1) из-за конкуренции с молекулами растворителя (значения констант см. в табл. 13). Для более длинных цепей модель "все или ничего" неприменима. В этих случаях необходимо вычислить статистическую сумму системы с помощью вероятностных методов, что и было сделано Дж. Эпплквистом и В. Дамлом [90] для модели "криво застегнутой молнии" ("staggering zipper"). Д. Пёршке [91] обработал экспериментальные данные в соответствии с этой моделью на ЭВМ.
Кинетика и механизм спаривания оснований. Пользуясь кинетическими данными, можно пролить свет на механизм кооперативного спаривания оснований. Для коротких спиралей однозначно подтверждается переход по типу "все или ничего". Релаксационный спектр состоит только из одной временной постоянной, которая относится к процессу второго, порядка типа "все или ничего", т. е. к рекомбинации обеих (комплементарных) цепей с образованием двойной спирали, имеющей максимальное число пар оснований. Только в случае более длинных цепей наблюдается дополнительный спектр постоянных времени первого порядка (τ << 1 мкс), который отражает изменения в конформациях с разомкнутыми концами или в зигзагообразных ("staggered") конформациях. Процесс второго порядка характеризуется большими скоростями рекомбинации, которые, однако, лежат ниже предела диффузионного контроля, указывая на порог нуклеации (kR: 106-107 M-1c-1). Значения этих констант скорости почти одинаковы для любой длины цепи больше трех (но меньше кооперативной длины). Они обнаруживают небольшую, но значимую зависимость от температуры, которая приводит к отрицательным кажущимся энергиям активации для АА-спиралей (pH ∼ 4), АУ-спиралей (нейтральная область, T < 50°С), а также для ГЦ-спиралей при более высокой температуре (Т > 50°С).
Абсолютные значения этих параметров "активации" позволяют совершенно непосредственно определить длину нуклеации. Если бы образование первой пары оснований лимитировало скорость*, то энергия активации (для процесса столкновения) была бы положительной. Поскольку мы знаем, что первая пара нестабильна (σ1s < 1 означает, что пара диссоциирует быстрее, чем образуется), следует ожидать наличия барьера нуклеации. Если этот барьер представляет собой только первую пару, т. е. если реакция "застегивания молнии" начинает распространяться, как только образуется стабильное ядро, состоящее из двух пар, то константа скорости должна иметь следующий вид: kR = σ1sk12, где k12 - константа скорости (первого порядка) образования второй пары (следующей за первой). Так как инкремент энергии активации для k12 должен быть положительным и σs имеет почти нулевой инкремент ΔH, а σ1s включает в лучшем случае малое отрицательное значение ΔH, то полная кажущаяся энергия активации должна быть близка к нулю, но не к экспериментально наблюдаемому значению 10 ккал/моль (например, для олигомеров АУ). Это относительно большое отрицательное значение совместимо только с выражением kR = σs2k23, описывающим процесс, в котором стадией, лимитирующей скорость, является образование третьей пары (k23). Таким образом, для последовательностей АУ стабильное ядро представляют собой спаренные триплеты оснований. Тогда константа скорости распространения (k23) будет равна примерно 107-108с-1 в согласии с наблюдаемыми временами релаксации ≤ 1 мкс для конфигураций с разомкнутыми концами. Олигомеры ГЦ при комнатной температуре могут образовывать стабильные "двухпарные ядра", так как их константы стабильности "s" значительно выше. Их константы рекомбинации дают положительные энергии активации, чего и следует ожидать, учитывая большие значения энергетических параметров (по сравнению с АУ). В кривых плавления они "маскируются" параметрами стопочного взаимодействия одиночных цепей (которые тоже выше).
* (Наблюдаются только те процессы, которые ведут к полным спиралям с максимальным числом пар оснований.)
Эти результаты подтверждаются независимыми определениями констант скорости диссоциации. Вследствие микроскопической обратимости
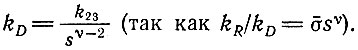 (IV.26)
(IV.26)Поскольку в знаменателе стоит sν-2, энергии активации положительны и включают в себя большой инкремент (ν - 2) ΔHs.
Ожидаемые значения и соответствующее уменьшение абсолютных значений kD с увеличением длины цепи (по порядку величины) наблюдаются в действительности.
IV.3.3. Выводы об узнавании. В табл. 13 собраны данные, полученные из равновесных и кинетических исследований, выполненных на олиго- и полирибонуклеотидах. Самое интересное явление - это предпочтение, отдаваемое триплету, причем не только по логически очевидным причинам (т. е. из-за того, что это дает возможность кодировать более чем 20 символов), а скорее вследствие механистических совпадений. Кодоны, состоящие из менее чем трех букв, были бы очень нестабильны (во всяком случае для А и У). Кодоны, состоящие из более чем трех букв, особенно в случае Г и Ц, были бы слишком "липкими". Время жизни пары кодон - антикодон не должно превышать несколько миллисекунд, чтобы создать возможность для оптимальной адаптации ферментов с соответствующими числами оборотов. Тот же тип оптимизации - компромисс между стабильностью и скоростью - всегда находят в случае фермент-субстратных взаимодействий. Любой выигрыш в стабильности означает снижение скорости диссоциации комплекса, которая должна регулироваться в соответствии с числом оборотов, чтобы не стать этапом, лимитирующим скорость всего процесса.

Таблица 14. Средние равновесные и кинетические параметры кооперативного спаривания оснований, полученные из релаксационных исследований с олигорибонуклеотидами (с длиной цепи от 3 до 18) в водной среде 1)
1) (Данные экстраполированы к 0°С и относятся к pH 7 и ионной силе 0,05 М (какодилат натрия) для АУ-пар и 0,1 М (фосфатный буфер, pH 7,2) для ГЦ-пар. Измерения Д. Пёршке [72, 73, 82, 91] и С. Поддера [76].)
2) (Экстраполировано к одиночным цепям без стопочного взаимодействия (реально измеренные значения, относящиеся к одиночным цепям со стопочным взаимодействием, значительно ниже).)
Замечание. Для констант скорости и равновесия даны только порядки величин, поскольку точные значения зависят от специальных сочетаний пар (кооперативность) и от условий опыта (ионная сила и т. д.).
Времена жизни для различных областей можно оценить, пользуясь значениями k23 (или k12) и s (или σsN соответственно).
Данные табл. 13 относятся в основном к спариванию в антикодоне, но включают, возможно, и другие открытые области. Эти значения выше, чем в табл. 14, вероятно, из-за стерической стабилизации петли антикодона. Следовательно, значения σ из этих данных экстраполировать нельзя. Ошибочное спаривание внутри области, в которой основания спарены, должно дать более низкие константы стабильности (находящиеся "на уровне шумов"), чем те, которые можно получить, пользуясь константами для ошибочного спаривания на концах (см. табл. 13).
Можно отметить еще одно интересное свойство триплета. Константы стабильности для комплементарных триплетов, полученные на олигомерных двойных спиралях с длиной цепи более чем ν = 4, оказываются значительно ниже тех, которые были определены непосредственно (в лаборатории П. Доти) по взаимодействию триплетов или квадруплетов оснований с открытыми областями тРНК. То же самое имеет место для параметров активации при спаривании Г с Ц, начиная с дублетной пары (см. положительные значения). По-видимому, в коротких открытых областях существуют более сильные стопочные взаимодействия, потому что пары оснований могут при этом расположиться так, чтобы получилось наиболее выгодное стопочное перекрывание. Часть этой энергии взаимодействия теряется, когда рассматриваемая область вытягивается в скрученную спиральную структуру, где на расположение пар оснований накладываются большие ограничения. (Такие же "стерические" ограничения относятся к "виляющей" паре ГУ, которая может образоваться только на одном из концов триплета.)
Если использовать данные, приведенные в табл. 14, можно сделать некоторые заключения относительно значений единичных факторов качества, которые определяют точность комплементарного инструктирования. Используя уравнение (IV.5), модифицированное для случая комплементарного взаимодействия, например для АУ (А - элемент матрицы),
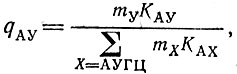 (IV.27)
(IV.27)получим значения, которые даже для оптимальных условий с трудом могут достигнуть 0,99. Точное определение потребовало бы более полной информации о константах стабильности для "ошибочных пар" внутри комплементарной области, и для различных комбинаций ближайших соседей. Для АУ эти величины, вероятно, значительно ниже 0,99, для ГЦ они могут быть - в определенных условиях - несколько выше: пара ГЦ всегда по меньшей мере в 10-50 раз более стабильна, чем пара АУ (в зависимости от ближайших соседей). Эти значения дают верхние пределы. Они предполагают, что в процессе комплементарного узнавания достигается равновесие, до того как мономер включится в полимерную цепь, и относятся к тому случаю, когда концентрации всех мономеров забуферены примерно до одного и того же значения. Такие условия вряд ли существуют в природе. Можно сделать вывод, что значения Q будут значительно отклоняться от единицы уже для относительно коротких цепей. Согласно уравнению (II.45), для воспроизводимого образования носителя кода Q должно оставаться выше определенного порогового значения. Таким образом, воспроизводимое образование нуклеиновых кислот с определенными последовательностями оснований без участия катализаторов было возможно только для относительно коротких цепей, содержащих, по-видимому, не больше 30-100 звеньев (для q = 0,99 и ν = 100 получим Q ≈ 1/е; см. табл. 8). Другая трудность - это механизм редупликации. Для сколько-нибудь точного узнавания комплементарных оснований требуются низкие температуры. При таких температурах образующиеся двойные спирали стабильны. Таким образом, для диссоциации спирали (что является непременным условием многократного матричного действия данной цепи) необходимы большие градиенты температуры. Поэтому большие различия в скоростях (которые существуют и в настоящее время, когда процессы репликации инструктируются ферментами) не могли бы возникнуть как следствие индивидуальной вторичной структуры.
Если, наконец, поставить вопрос:
Могут ли нуклеиновые кислоты организовать самореплицирующуюся и эволюционирующую единицу без содействия катализаторов?
То следует ответить:
Вследствие комплементарных взаимодействий каждый коллектив, состоящий из положительной и отрицательной цепи, обладает способностью к самоинструктированию. При благоприятных условиях среди них мог бы происходить отбор отдельных коллективов с определенными последовательностями. Однако эти последовательности - если они вообще воспроизводимо образуются - содержат очень малое количество информации (ν < 100). Так как различные коллективы должны конкурировать друг с другом, такая система (без помощи самоинструктирующихся катализаторов) не смогла бы достигнуть такого уровня организации, на котором возможно согласованное функционирование.
|
ПОИСК:
|
© GENETIKU.RU, 2013-2022
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'
При использовании материалов активная ссылка обязательна:
http://genetiku.ru/ 'Генетика'